题目内容
1.将4.0gCu-Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应.过滤、称量滤液的质量.相关实验数据如表:| 反应前物质质量/g | 反应后物质质量/g | |
| Cu-Zn合金 | 稀硫酸 | 滤液质量 |
| 4.0 | 10 | 11.26 |
(2)请计算Cu-Zn合金中Zn的质量分数.
分析 本题不能直接得到氢气的质量,但是由于给出了硫酸以及所以滤液的质量,所以可以根据溶液质量差量来计算锌的质量,进而求算其质量分数.
解答 解:Cu-Zn合金属于金属材料.
设合金中锌的质量为x
Zn+H2SO4=ZnSO4+H2↑ 溶液质量变化
65 98 161 161-98=63
x 11.26g-10g=1.26g
$\frac{65}{63}$=$\frac{x}{1.26g}$
x=1.3g
则Cu-Zn合金中Zn的质量分数为$\frac{1.3g}{4g}$×100%=32.5%
答:(1)Cu-Zn合金属于金属材料.
(2)Cu-Zn合金中Zn的质量分数为32.5%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
9.下列四个实验方案设计不合理的是( )
| 选项 | 实验目的 | 方案 |
| A | 除去固体氯化钙中少量的碳酸钙 | 加水溶解后,过滤、蒸发 |
| B | 鉴别NHCl溶液和K2SO4溶液 | 加入NaOH溶液 |
| C | 除去NaCl溶液中的Na2CO3 | 加入适量硝酸钙溶液、过滤 |
| D | 比较Fe、Cu、Ag的金属活动性 | 铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.我国学者发现了稳定的氦氮化合物,有关氦、氮元素相关信息如图,下列有关说法错误的是( )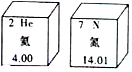

| A. | 都属于非金属元素 | B. | 氦元素的核内电子数为2 | ||
| C. | 氮元素在空气中含量最高 | D. | 氦元素的相对原子质量为4.00 |
13.下列图示实验基本操作错误的是( )
| A. | 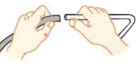 | B. | 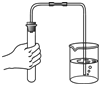 | C. | 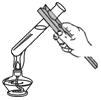 | D. | 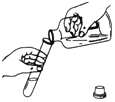 |
10.下列各选项的能量转化过程中,主要发生化学变化的是( )
①太阳能供热②核反应发电③火力发电④电热器取暖⑤火药爆炸.
①太阳能供热②核反应发电③火力发电④电热器取暖⑤火药爆炸.
| A. | ①② | B. | ③④ | C. | ②③⑤ | D. | ③⑤ |
11.超轻水,又称“低氘水”.它是采用高科技制造技木.降低自然界水中的氘含量而生产的高端饮用水.目前超轻水在欧美、日本已经被广泛地用于癌症防治、保健界生、美容护理等领域.下列关于超轻水的说法中正确的是( )
| A. | 超轻水不属于氧化物 | B. | 超轻水和普通水的化学性质相同 | ||
| C. | 超轻水中水分子不运动 | D. | 长期饮用超轻水对身体没有益处 |
