题目内容
某氯化钠废水中含有HCl,H2SO4,Na2SO4,现在要回收NaCl,得到纯净NaCl的晶体,实验室进行提纯的流程如图:
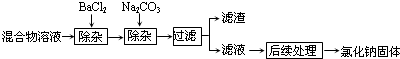
回答下列问题:
(1)加入Na2CO3溶液,目的是除去溶液中存在的 和 (填离子符号).
(2)滤渣的主要成分是 (填化学式).
(3)为了获得纯净的氯化钠晶体,“后续处理”的主要操作是①先 ②然后 ,进行该操作时,当出现 就停止加热.利用余热把固体蒸干.写出其中反应的化学方程式 .

回答下列问题:
(1)加入Na2CO3溶液,目的是除去溶液中存在的
(2)滤渣的主要成分是
(3)为了获得纯净的氯化钠晶体,“后续处理”的主要操作是①先
考点:混合物的分离方法,蒸发与蒸馏操作,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯
分析:(1)根据碳酸钠和氯化钡反应及稀盐酸的反应分析解答;
(2)根据硫酸和硫酸钠都能和氯化钡反应生成硫酸钡沉淀,碳酸钠和氯化钡生成碳酸钡沉淀解答;
(3)根据滤液中含有过量的碳酸钠和氯化钠所以先加稀盐酸除去碳酸钠再蒸发结晶,当出现较多固体时停止加热,碳酸钠和稀盐反应生成氯化钠、水和二氧化碳解答.
(2)根据硫酸和硫酸钠都能和氯化钡反应生成硫酸钡沉淀,碳酸钠和氯化钡生成碳酸钡沉淀解答;
(3)根据滤液中含有过量的碳酸钠和氯化钠所以先加稀盐酸除去碳酸钠再蒸发结晶,当出现较多固体时停止加热,碳酸钠和稀盐反应生成氯化钠、水和二氧化碳解答.
解答:解:(1)碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,碳酸钠和稀盐酸的反应生成氯化钠、水和二氧化碳,所以加入碳酸钠除去的是钡离子和氢离子;
(2)硫酸和硫酸钠都能和氯化钡反应生成硫酸钡沉淀,碳酸钠和氯化钡生成碳酸钡沉淀;
(3)滤液中含有过量的碳酸钠和氯化钠所以先加稀盐酸除去碳酸钠再蒸发结晶,当出现较多固体时停止加热,碳酸钠和稀盐反应生成氯化钠、水和二氧化碳.
故答案:(1)Ba2+、H+;(2)BaCO3、BaSO4;(3)①先往滤液中加入过量的稀盐酸(或逐滴滴入稀盐酸至不再产生气泡为止),②蒸发(结晶);
较多固体;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)硫酸和硫酸钠都能和氯化钡反应生成硫酸钡沉淀,碳酸钠和氯化钡生成碳酸钡沉淀;
(3)滤液中含有过量的碳酸钠和氯化钠所以先加稀盐酸除去碳酸钠再蒸发结晶,当出现较多固体时停止加热,碳酸钠和稀盐反应生成氯化钠、水和二氧化碳.
故答案:(1)Ba2+、H+;(2)BaCO3、BaSO4;(3)①先往滤液中加入过量的稀盐酸(或逐滴滴入稀盐酸至不再产生气泡为止),②蒸发(结晶);
较多固体;Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评:分离不溶于液体的固体与液体用过滤的方法,本题考查物质分离、提纯实验方案的设计,把握流程中试剂的加入发生的化学反应及操作为解答的关键,注重实验的严密性和溶液的配制、物质提纯的考查,题目难度中等.

练习册系列答案
相关题目
目前,农村常用的化肥有:NH4HCO3、NH4NO3、KNO3、CO(NH2)2(尿素)、KH2PO4、KCl、Ca(H2PO4)2、NH4H2PO4等,下列化肥属于复合肥料的是( )
| A、NH4HCO3 |
| B、KNO3 |
| C、Ca(H2PO4)2 |
| D、NH4NO3 |