题目内容
在密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 20 | 5 |
| 反应后质量/g | 10 | 8 | 13 | 未知 |
| A、反应后未知的质量为6g |
| B、该反应类型一定是置换反应 |
| C、参加反应的物质为Z和Q |
| D、Y与Q的相对分子质量比一定为1:1 |
考点:质量守恒定律及其应用,反应类型的判定
专题:化学用语和质量守恒定律
分析:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,即8+2+20+5=未知+10+8+13,得未知的质量为4g;根据反应后质量增加的是生成物,减少的是反应物,结合表格信息可乙判断,生成物是X和Y,反应物是Z和Q,从而可以求得参加反应的Y与Q的相对分子质量,从而可以正确求解.
解答:解:根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,即8+2+20+5=未知+10+8+13,得未知的质量为4g;
A、由上述分析可知待测的质量为4g,故A错;
B、由上述分析可知,生成物是X和Y,反应物是Z和Q,因为无法知道物质的分类,则无法推测反应类型是否是置换反应,故B错;
C、由上述分析可知,反应物是Z和Q,故C对;
D、参加反应的Y、Q的质量之比为(8g-2g):(5g-4g)=6:1,因为不知化学方程式的二者的计量数,则二者的相对分子质量之比不一定为1:1;故D错.
故选C.
A、由上述分析可知待测的质量为4g,故A错;
B、由上述分析可知,生成物是X和Y,反应物是Z和Q,因为无法知道物质的分类,则无法推测反应类型是否是置换反应,故B错;
C、由上述分析可知,反应物是Z和Q,故C对;
D、参加反应的Y、Q的质量之比为(8g-2g):(5g-4g)=6:1,因为不知化学方程式的二者的计量数,则二者的相对分子质量之比不一定为1:1;故D错.
故选C.
点评:本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.仔细推敲,即可求解.

练习册系列答案
相关题目
下列粒子结构示意图中,表示阳离子的是( )
A、 |
B、 |
C、 |
D、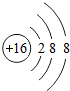 |
化学实验操作的正确性、规范性是科学探究成败的关键因素之一.下列实验操作中,正确的是( )
A、 加热液体 |
B、 塞紧橡皮塞 |
C、 稀释浓硫酸 |
D、 测定溶液的pH 测定溶液的pH |
植物的光合反应可以用下式表示:6H2O+6CO2
C6H12O6+6O2,在该反应中,若植物吸收了54gH2O和132gCO2,那么在生成90gC6H12O6的同时,释放的氧气质量为( )
| 叶绿素 |
| 阳光 |
| A、54g | B、90g |
| C、96g | D、132g |
下列有关实验操作中“量”的说法错误的是( )
| A、实验中没有规定取用药品的量时,可以按任意量取用 | ||
B、给试管中的液体加热,液体的量不能超过试管容积的
| ||
C、酒精灯内的酒精量最多不超过酒精灯容积的
| ||
D、洗涤试管时,可注入
|
下列试剂瓶标签上的化学式书写错误的是( )
A、 |
B、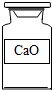 |
C、 |
D、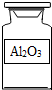 |
下列叙述不正确的是( )
| A、分子、原子和离子都能直接构成物质 |
| B、原子中原子核与核外电子的电量相等,电性相反,因而原子不显电性 |
| C、分子和原子的根本区别是,分子可分、原子不可分 |
| D、原子如果得到或失去电子就变成了离子 |
下列实验操作中,正确的是( )
A、 |
B、 |
C、 |
D、 |
 硅元素在现代信息技术产业有着广泛的应用,如图摘自元素周期表,请你将如图能提供的关于硅元素的信息
硅元素在现代信息技术产业有着广泛的应用,如图摘自元素周期表,请你将如图能提供的关于硅元素的信息