题目内容
如图是一个密闭体系中某反应的微观示意图:
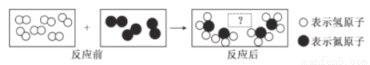
(1)反应后还应再填入一个下列哪种物质的微粒_____(填序号);
A.H2 B.HN3 C.NH3 D.N2
(2)该反应属于_____反应(填基本反应类型),反应后的物质是_____(填“混合物”或“纯净物”);
(3)参加反应的“○○”和“●●”分子个数比是____。
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好,小菁决定对影响碳酸钠溶液碱性的因素展开探究,请你参与。用不同温度的水,配制溶质质量分数分别为2%、6%和10%的碳酸钠溶液,依次测量溶液pH,记录数据如下表:
实验编号 | a1 | a2 | a3 | b1 | b2 | b3 | c1 | c2 | c3 |
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
请你分析表中数据回答:
(1)溶液碱性最强的是__________(填实验编号)。
(2)要得出碳酸溶液的溶质质量分数变化与pH变化关系的结论,可选择的一组实验是_______(填实验编号),结论是________________________________________。
(3)将10%的碳酸钠溶液从20℃持续升温到70℃,所测得的pH如下表:
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 |
溶液pH | 11.22 | 11.35 | 11.46 | 11.48 | 11.50 | 11.50 |
①当温度介于20℃~40℃时,温度对碳酸钠溶液的pH影响比较__________(选填“大”或“小”)。
②小菁将适量碳酸钠粉末洒在有油污的餐具上,并冲入适量的热水,再进行擦洗,达到较好的洗涤效果,这是因为__________________________________________________。
(4)欲使碳酸钠溶液中的碳酸钠完全转化为烧碱,可在溶液中加入一定量的物质,并充分搅拌,有关反应的化学方程式为________________________________________。
“舌尖上的中国”热播以来,让众多吃货为之疯狂。厨房里的大师们在炒菜时,加料酒后又加醋,就让菜肴变得香美可口,这其实隐藏了一个化学的小秘密:醋中的乙酸与料酒中的乙醇反应生成有香味的乙酸乙酯。下表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为_______;其中碳元素的质量分数为_______;
(2)比较归纳是学习化学的重要方法,据表推测X的化学式为_______;
(3)若菜肴中的乙酸乙酯在体内代谢时,其所含的碳元素完全转化为CO2,则44mg的乙酸乙酯完全代谢产生的CO2的质量为多少_______?(请写出计算过程)