题目内容
11.某化工厂用石灰石和废铜屑等设计生产石青、波尔多液的工艺流程如下:
(1)X的化学式为CO2.
(2)反应②中空气的作用是起氧化作用.
(3)若反应④中硫酸铜、生石灰和水的化学计量数之比为1:1:1,则其反应的化学方程式为:
CuSO4+CaO+H2O═Cu(OH)2+CaSO4.
分析 (1)根据碳酸钙高温分解会生成氧化钙和二氧化碳,质量守恒定律中的元素、原子守恒进行分析;
(2)根据反应②的反应物、生成物以及反应原理进行分析;
(3)根据反应④中硫酸铜、生石灰和水的化学计量数之比为1:1:1,依据质量守恒定律书写化学方程式.
解答 解:(1)石灰石在高温的条件下会生成氧化钙和二氧化碳,所以X是二氧化碳,化学式为:CO2;
(2)通过分析反应原理可知,铜和氧气加热生成氧化铜,氧化铜和稀硫酸反应生成硫酸铜和水,空气在反应中是提供氧,所以反应②中空气的作用是:起氧化作用;
(3)反应④中硫酸铜、生石灰和水的化学计量数之比为1:1:1,硫酸铜、生石灰和水反应生成氢氧化铜沉淀和硫酸钙,化学方程式为:CuSO4+CaO+H2O=Cu(OH)2↓+CaSO4.
故答案为:(1)CO2;
(2)起氧化作用;
(3)CuSO4+CaO+H2O═Cu(OH)2+CaSO4.
点评 在解此类题时,首先分析题中的反应原理,然后依据学过的知识和题中的知识进行解答即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1. 一包黑色粉末可能由氧化铜和炭粉中的一种或两种物质组成,某学校科学小组为确定其成分,进行了以下探究活动:
一包黑色粉末可能由氧化铜和炭粉中的一种或两种物质组成,某学校科学小组为确定其成分,进行了以下探究活动:
【查阅资料】硫酸铜溶液呈蓝色
【设计方案】(1)取少量黑色粉末于试管中$\frac{满加足量稀硫酸}{加热}$观察现象
实验中可能出现的现象与对应结论如下表,请你完成下表中①②相关内容:
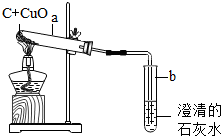
(2)通过实验及分析,确定该粉末为氧化铜和炭粉的混合物,为了进一步探究它们的性质,探究小组又利用这种混合物补充做了如图所示实验:
①能证明CuO与C已发生化学反应的实验现象是
a黑色粉末中有红色粉末出现,b试管内澄清的石灰水变浑浊.
试管b中反应的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
②最能说明a试管中物质已完全反应的实验现象是不再有气泡产生.
 一包黑色粉末可能由氧化铜和炭粉中的一种或两种物质组成,某学校科学小组为确定其成分,进行了以下探究活动:
一包黑色粉末可能由氧化铜和炭粉中的一种或两种物质组成,某学校科学小组为确定其成分,进行了以下探究活动:【查阅资料】硫酸铜溶液呈蓝色
【设计方案】(1)取少量黑色粉末于试管中$\frac{满加足量稀硫酸}{加热}$观察现象
实验中可能出现的现象与对应结论如下表,请你完成下表中①②相关内容:
| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含①C |
| 溶液呈蓝色,②无黑色不溶物. | 只含CuO |
①能证明CuO与C已发生化学反应的实验现象是
a黑色粉末中有红色粉末出现,b试管内澄清的石灰水变浑浊.
试管b中反应的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
②最能说明a试管中物质已完全反应的实验现象是不再有气泡产生.
6.下列叙述中,错误的是( )
| A. | 铵态氮肥不能与草木灰(主要成分是碳酸钾)混合施用 | |
| B. | 在煤中加入石灰石和生石灰作固硫剂以减少空气污染 | |
| C. | 在图书档案、贵重设备、精密仪器等发生火灾时,可用泡沫灭火器扑灭 | |
| D. | 含碳酸氢钠的药物可以治疗胃酸过多症 |
16.如图是某化学反应的微观模拟示意图,正确的判断是( )
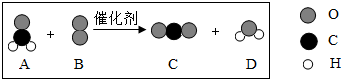

| A. | 该反应属于置换反应 | |
| B. | 反应前后原子的种类、个数没有发生变化 | |
| C. | 其中三种物质属于氧化物 | |
| D. | 此反应中B与C的质量比为1:1 |
3.如图为甲、乙两种固体物质的溶解度曲线,下列叙述不正确的是( )
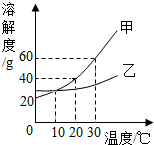

| A. | 甲、乙两种物质均属于易溶物质 | |
| B. | 甲物质的溶液度受温度变化的影响较大 | |
| C. | 在20℃时,甲、乙两种物质的饱和溶液中溶质的质量相等 | |
| D. | 当甲中含有少量的乙时,可用降温结晶法提纯 |
20.千姿百态的物质世界存在多种相互作用,也不断发生变化.下列属于化学变化的是( )
| A. | 冰雪融化 | B. | 玻璃破碎 | C. | 食物腐烂 | D. | 气球爆炸 |
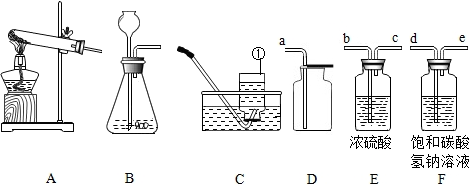
 实验桌上摆放着四种试剂,请选取适当的试剂回答下列问题.
实验桌上摆放着四种试剂,请选取适当的试剂回答下列问题.