题目内容
20.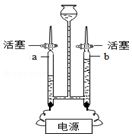 用如图装置进行水的电解实验:
用如图装置进行水的电解实验:(1)在水中加入稀硫酸或氢氧化钠,其作用是增强水的导电性.
(2)开始反应前a、b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,写出电解水的文字表达式水$\stackrel{通电}{→}$氧气+氢气;可推得水是由氢、氧元素组成的.
(3)若实验中用4%的氢氧化钠溶液100g,通电一段时间后,氢氧化钠溶液溶质质量分数变为6.25%,则分解水的质量为36g.
分析 (1)根据稀硫酸或氢氧化钠在水中能解离出自由移动的离子分析;
(2)根据电解水的反应和结论分析回答;
(3)根据溶质质量不变原理分析计算.
解答 解:(1)由于稀硫酸或氢氧化钠在水中能解离出自由移动的离子,在水中加入稀硫酸或氢氧化钠,其作用是增强水的导电性.
(2)电解水生成了氢气和氧气,反应的文字表达式是:水$\stackrel{通电}{→}$氧气+氢气;可推得水是由氢、氧元素 组成的;
(3)设分解水的质量为x,则:
100g×4%=(100g-x)×6.25% 解得:x=36g.
故答为:(1)增强水的导电性;(2)水$\stackrel{通电}{→}$氧气+氢气;氢、氧元素;(3)36.
点评 本题主要考查了电解水的反应、注意事项、结论和溶质质量分数的简单计算,属于基础的知识,根据已有的知识分析解答即可.

练习册系列答案
相关题目
10.某学习小组同学用过氧化氢溶液制取氧气.
(1)如表是分解等量的过氧化氢溶液时选用不同催化剂所得到的实验数据:
从上述数据可得出一个结论:在该反应中二氧化锰的催化效果最好.
(2)取含过氧化氢1.7g的溶液,加入适量催化剂充分反应,计算能得到氧气的质量.
(1)如表是分解等量的过氧化氢溶液时选用不同催化剂所得到的实验数据:
| 催化剂(质量均为0.3g) | 新鲜猪肝 | CuCl2 | MnO2 | CuO |
| 收集1L氧气所需的时间(s) | 42 | 650 | 18 | 300 |
(2)取含过氧化氢1.7g的溶液,加入适量催化剂充分反应,计算能得到氧气的质量.
15.自然界中的水都不是纯净物,下列方法能得到纯净水的是( )
| A. | 吸附 | B. | 沉淀 | C. | 过滤 | D. | 蒸馏 |
5.把铝箔放入CuCl2溶液中,铝箔表面覆盖了红色物质,一会儿又有大量气泡冒出.同学们对“放出气体”这一异常现象进行猜想、实验.其中没有价值的是( )
| A. | 小寒同学认为气体是氨气并检验 | |
| B. | 小琪同学猜想CuCl2溶液呈酸性并测定 | |
| C. | 小宇同学推测气体是氢气并检验 | |
| D. | 小梁同学认为试剂变质,更换后再实验 |
14.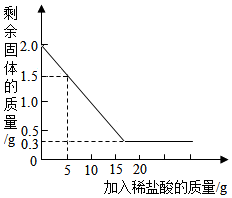 某石灰厂有一批石灰石原料,其中含有的杂质为二氧化硅(二氧化硅不溶于水,不与盐酸反应.高温时比发生分解)为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,用实验室未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:
某石灰厂有一批石灰石原料,其中含有的杂质为二氧化硅(二氧化硅不溶于水,不与盐酸反应.高温时比发生分解)为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,用实验室未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:
计算:(1)分析上述图与表,第二次加入稀盐酸后,剩余的固体的质量是1.0克.
( 2 )该石灰石样品中含碳酸钙的质量是1.7克;
(3)所用稀盐酸的溶质质量分数是多少?
 某石灰厂有一批石灰石原料,其中含有的杂质为二氧化硅(二氧化硅不溶于水,不与盐酸反应.高温时比发生分解)为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,用实验室未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:
某石灰厂有一批石灰石原料,其中含有的杂质为二氧化硅(二氧化硅不溶于水,不与盐酸反应.高温时比发生分解)为了测定该石灰石的纯度,兴趣小组的同学取用2g这种石灰石样品,用实验室未知溶质质量分数的稀盐酸20g分4次加入,充分反应后,经过滤、干燥等操作后,根据每次稀盐酸用量及剩余固体质量和实验数据绘制成图象(如图).计算:| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5克 | 1.5克 |
| 第二次加入5克 | 1.0g |
| 第三次加入5克 | 0.5克 |
| 第四次加入5克 | 0.3克 |
( 2 )该石灰石样品中含碳酸钙的质量是1.7克;
(3)所用稀盐酸的溶质质量分数是多少?
 某化肥包装袋上的部分说明如图所示.请你完成下列各题:
某化肥包装袋上的部分说明如图所示.请你完成下列各题: