题目内容
1.已知硫酸铵的化学式为(NH4)2SO4计算(要求列式并计算)(1)(NH4)2SO4的各元素的原子个数比;
(2)相对分子质量;
(3)组成各元素的质量比;
(4)氮元素的质量分数;
(5)132克硫酸铵中氮元素的质量为多少克.
分析 (1)根据1个硫酸铵分子的构成进行分析解答.
(2)根据相对分子质量等于化学式中各原子的相对原子质量的总和进行解答.
(3)化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)1个硫酸铵分子是由2个氮原子、8个氢原子、1个硫原子、4个氧原子构成的,则(NH4)2SO4中氮、氢、硫、氧四种元素的原子个数比为2:8:1:4.
(2)硫酸铵的相对分子质量=(14+1×4)×2+32+16×4=132.
(3)硫酸铵中氮、氢、硫、氧四种元素的质量比为(14×2):(1×8):32:(16×4)=7:2:8:16.
(4)氮元素的质量分数为$\frac{14×2}{132}$×100%≈21.2%.
(5)132克硫酸铵中氮元素的质量为132g×$\frac{14×2}{132}$×100%=28g;
答:(1)(NH4)2SO4中氮、氢、硫、氧四种元素的原子个数比为2:8:1:4;
(2)硫酸铵的相对分子质量是132;
(3)硫酸铵中氮、氢、硫、氧四种元素的质量比为7:2:8:16;
(4)硫酸铵中氮元素的质量分数为21.2%;
(5)132克硫酸铵中氮元素的质量是28g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.区分下列各组物质,所加试剂或操作方法完全正确的是( )
| 需鉴别物质 | 方法Ⅰ | 方法Ⅱ | |
| A | 白醋和白酒 | 闻气味 | 品尝 |
| B | 一氧化碳和二氧化碳 | 闻气味 | 通过灼热的氧化铁 |
| C | 食盐水和蒸馏水 | 看颜色 | 蒸发 |
| D | 真黄金和假黄金(铜锌合金) | 看颜色 | 灼烧 |
| A. | A | B. | B | C. | C | D. | D |
10.在化学反应A2+3B2═2AB3,6gB2与足量的A2反应后,得34gAB3,则化合物中A、B两物质质量之比是( )
| A. | 17:4 | B. | 14:3 | C. | 14::7 | D. | 14:17 |
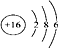 表示S的原子结构示意图.
表示S的原子结构示意图.