��Ŀ����
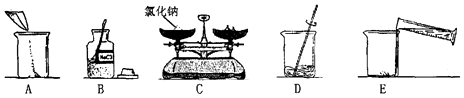
����Ŀ����ͼ������������������Ϊ20%��NaCl��Һ��ʵ�����ʾ��ͼ�� 
��1������ͼ��ʾ����ű�ʾ������Һ����ȷ����˳�� ��
��2�����ݼ�����Ҫ��ȡˮ�������Ͳ�Ĺ��������������ѡ�ã�200mL��50mL��100mL��������������̶ȳߣ�
��3����������Һ�Ĺ����У������Ȼ�����������С��20%�Ŀ���ԭ��������ţ�
A.����Ͳ��ȡˮʱ���Ӷ���
B.����ǰָ������ƫ�ƾͳ���
C.������Һ���ձ���������ˮ��ϴ
D.װƿʱ����Һ������
E.�Ȼ��Ʋ�����
���𰸡�
��1���ڢݢ٢ܢ�
��2��100mL
��3��BCF
���������⣺��1������������������Ϊ10%��NaCl��Һ�IJ����ǣ����㡢��������ȡ���ܽ⣻����ڢݢ٢ܢۣ���2����Һ������Ϊ��15g��20%=90g��ˮ������Ϊ��90g��15g=75g����75mL��������Ҫ100mL����Ͳ�����100mL����3��A������Ͳ��ȡˮʱ���Ӷ�������������ȡˮ���ƫС������������������ƫ��
B������ǰָ������ƫ�ƾͳƣ����³�ȡ��ҩƷƫ�٣�����������������ƫС��
C��������Һ���ձ�����������ˮ��ϴ��ʹ��ȡˮ�������ӣ�����������������ƫС��
D����Һ���ձ���ú�ת�Ƶ��Լ�ƿ��ʱ�������伸�Σ���Һ���о�һ�ԣ��������Һ����Ӱ����Һ������������
F���Ȼ��ƾ��岻������ʹ��������������һ����Ϊ���������������Ȼ�������ƫС������������������ƫС��
���BCF��