题目内容
有关资料介绍,制取氧气有多种方法,其中氧化铜与氯酸钾混合加热,也能很快产生氧气。现将2.5g氧化铜与24.5g氯酸钾的混合物充分加热,残余固体经冷却、称量、质量为17.4g。然后将固体溶于65.1 g水中,充分搅拌,过滤得到滤液和黑色的滤渣。滤渣又经过洗涤、烘干、称量,质量为2.5g。( 不考虑过程中物质的损失,计算结果保留一位小数)
不考虑过程中物质的损失,计算结果保留一位小数)
(1)该反应中氧化铜起 作用。
(2)生成的氧气为 克。
(3)所得滤液中溶质是 ,其质量分数为 。
(4)向所得滤液中加入质量分数为16%的AgNO3溶液恰好完全反应,需AgNO3溶液的质量为多少克?(列出必要的计算过程)
 (1)催化 (2)9.6 (3)氯化钾 18.6%
(1)催化 (2)9.6 (3)氯化钾 18.6%
(4)设需要AgNO3的质量是x
KCl + AgNO3 === AgCl↓ + KNO3
74.5 170
14.9g X
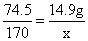
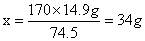
需要AgNO3溶液的质量是: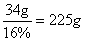
答:需要AgNO3溶液的质量是225g。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目



 、
、 的粒子,表示了同种元素不同的粒子
的粒子,表示了同种元素不同的粒子 ,由此可写出各步反应的化学方程式。
,由此可写出各步反应的化学方程式。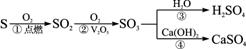 。
。 :____;反应③:____。
:____;反应③:____。 扇越旺,蜡烛一扇就灭,以下对该现象的分析正确的是
扇越旺,蜡烛一扇就灭,以下对该现象的分析正确的是