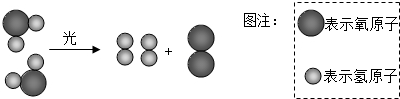题目内容
15.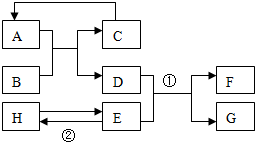 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据右图的转化关系(反应条件均已略去):
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能产生温室效应;B为红棕色,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据右图的转化关系(反应条件均已略去):(1)写出下列物质的化学式:BFe2O3、CCO2;
(2)写出下列反应的化学方程式:A+B-C+D3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;②CuSO4+2NaOH=Cu(OH)2↓+Na2SO4(CuCl2等也行).
分析 根据题目中的突破口C能产生温室效应”,所以C是二氧化碳,A、C是组成元素相同的气体,所以A是一氧化碳,“B为红棕色,是赤铁矿的主要成分”、所以B是氧化铁,“F是紫红色金属,故F是铜;H是蓝色沉淀”,H是氢氧化铜沉淀,再进一步进行分析即可.
解答 解:C能产生温室效应”,所以C是二氧化碳,A、C是组成元素相同的气体,所以A是一氧化碳,“B为红棕色,是赤铁矿的主要成分”、所以B是氧化铁,一氧化碳还原氧化铁生成二氧化碳和铁,故C是二氧化碳,D为铁,H是蓝色沉淀”,故H是氢氧化铜沉淀,“F是紫红色金属,故F是铜;D与E反应产生铜,故E为铜盐溶液,由E铜盐溶液制取氢氧化铜可跟碱溶液反应.因此:
(1)由上述分析可知B是氧化铁,C是二氧化碳,故填:Fe2O3、CO2;
(2)A+B-C+D反应是一氧化碳还原氧化铁反应产生铁和二氧化碳,故反应的方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
反应②是铜盐溶液与碱反应可制取氢氧化铜沉淀,如硫酸铜和氢氧化钠反应产生氢氧化铜沉淀和硫酸钠,故反应的方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 (CuCl2等也行).
点评 本题为框图式推断题,解答本题关键是要找出突破口,知道造成温室效应的主要气体是二氧化碳,赤铁矿的主要成分是氧化铁,紫色金属是铜,蓝色沉淀是氢氧化铜,再根据学过去的知识进一步进行分析推断即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.下列资源的利用过程中发生了化学变化的是( )
| A. | 铁矿炼铁 | B. | 干冰制冷 | C. | 太阳能供电 | D. | 海水晒盐 |
10.如图为某化工企业生产流程示意图,有关说法正确的是( )
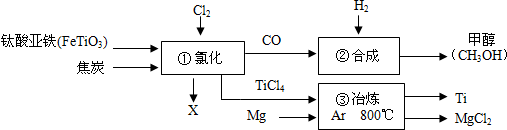

| A. | ?中氩气(Ar)作反应物 | |
| B. | 钛酸亚铁(FeTiO3)中钛元素为+3价 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2的质量比为14:1 | |
| D. | ①中反应为:2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,则X为FeCl3 |
5.下面是对四个实验绘制的图形,其中实验结果与对应图形正确的是( )
| A. | 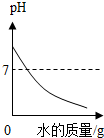 向pH=13的NaOH溶液中加入水 | |
| B. | 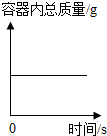 在密闭容器中加热高锰酸钾 | |
| C. | 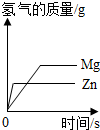 等质量的镁粉、锌粉与足量的同浓度的稀硫酸反应 | |
| D. | 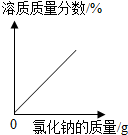 常温下,一定量的水中溶解氯化钠 |
 如图为某反应的微观示意图.图中“
如图为某反应的微观示意图.图中“ 、
、 ”代表不同元素的原子.依据图示回答问题:
”代表不同元素的原子.依据图示回答问题: