题目内容
2.化学小组应用如图所示的装置进行相关实验(夹持仪器略去,K1、K2、K3均关闭,装置内所示药品的量可认为是实验中某一状态下的量),已知装置内的药品,甲:稀盐酸;乙中为无色气体;分液漏斗中为红色的溶液;丙:石灰水,依据相关信息回答问题:(碳酸钠溶液呈碱性)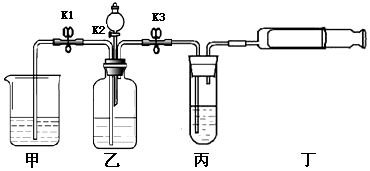
(1)打开K3,将丁向外拉,丙中长导管口有气泡冒出,且出现白色浑浊现象,则乙中的无色气体是二氧化碳,丙中出现白色浑浊的原因是Ca(OH)2+CO2═CaCO3↓+H2O.(用化学方程式回答)
(2)关闭K3,打开K2(分液漏斗上端的玻璃塞处于打开状态),当分液漏斗内的红色溶液全部进入到乙中时,关闭K2,振荡乙一会儿后,打开K1,可观察到甲中的现象是甲中溶液进入乙中,乙中有气体产生,且溶液由红色变为无色,产生气体的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑,从物质性质的角度解释溶液由红色变为无色的原因是稀盐酸与碱性溶液发生反应,使溶液失去了碱性.
分析 (1)二氧化碳能使澄清石灰水变浑浊,是因为二氧化碳能和澄清石灰水中的氢氧化钙反应生成碳酸钙沉淀和水;
(2)氢氧化钠溶液显碱性,能使酚酞试液变红色,能和二氧化碳反应生成碳酸钠和水;
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳.
解答 解:(1)打开K3,将丁向外拉,丙中长导管口有气泡冒出,且出现白色浑浊现象,则乙中的无色气体是二氧化碳,丙中出现白色浑浊的原因是:二氧化碳进入澄清石灰水中,和氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:二氧化碳;Ca(OH)2+CO2═CaCO3↓+H2O.
(2)关闭K3,打开K2,当分液漏斗内的红色溶液全部进入到乙中时,关闭K2,振荡乙一会儿后,氢氧化钠和二氧化碳反应生成了碳酸钠和水,导致乙中压强减小,打开K1,可观察到甲中溶液进入乙中,乙中有气体产生,是因为稀盐酸和碳酸钠反应生成了二氧化碳,反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
溶液由红色变为无色,是因为稀盐酸与碱性溶液发生反应,使溶液失去了碱性,酚酞试液由红色变成无色.
故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑;稀盐酸与碱性溶液发生反应,使溶液失去了碱性.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列物质中,属于纯净物的是( )
| A. | 矿泉水 | B. | 海水 | C. | 自来水 | D. | 蒸馏水 |
14. a、b两种物质的溶解度曲线如图所示,下列说法错误的是( )
a、b两种物质的溶解度曲线如图所示,下列说法错误的是( )
 a、b两种物质的溶解度曲线如图所示,下列说法错误的是( )
a、b两种物质的溶解度曲线如图所示,下列说法错误的是( )| A. | 15℃时,a、b的溶解度均为20g | |
| B. | 15℃时,将15gb放入50g水中,充分溶解后,所得溶液质量是65g | |
| C. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| D. | 将30℃时a的饱和溶液降温至15℃,溶质的质量分数不变 |
11.从物质变化的角度分析,下列典故主要体现化学变化的是( )
| A. | 火烧赤壁 | B. | 凿壁偷光 | C. | 悬梁刺股 | D. | 刻舟求剑 |
18.用数轴表示某些化学知识直观、简明、易记,下列表达正确的是( )
| A. | 少$→_{空气中物质的体积分数}^{N_{2}CO_{2}O_{2}}$多 | |
| B. | 弱$→_{金属的活动性}^{FeMgCu}$ | |
| C. | 小$→_{相对分子质量}^{H_{2}H_{2}OH_{2}O_{2}}$大 | |
| D. | 小$→_{溶液的pH}^{NaOHH_{2}SO_{4}NaCl}$大 |
7.下列实验中的玻璃棒没有起到搅拌作用的是( )
| A. | 测定溶液的pH | B. | 溶解固体 | C. | 蒸发溶液 | D. | 稀释浓硫酸 |
14.下列图象与对应的叙述相符合的是( )
| A. | 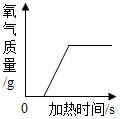 加热一定质量的高锰酸钾 | |
| B. | 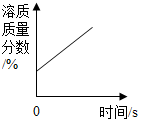 将一瓶浓硫酸敞口放置在空气中 | |
| C. | 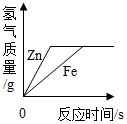 向等质量等溶质质量分数的稀盐酸中分别加入过量的锌和铁 | |
| D. | 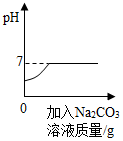 向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液 |
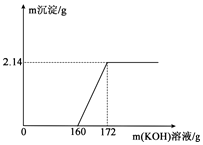 工业盐酸中通常溶有少量的FeCl3而呈黄色,为了测定某工业盐酸中HCl的含量进行如下实验,同学取某工业盐酸100g,滴加一定溶质质量分数的KOH,测得加入KOH溶液质量与反应生成的沉淀质量关系如图所示.请回答下列问题:
工业盐酸中通常溶有少量的FeCl3而呈黄色,为了测定某工业盐酸中HCl的含量进行如下实验,同学取某工业盐酸100g,滴加一定溶质质量分数的KOH,测得加入KOH溶液质量与反应生成的沉淀质量关系如图所示.请回答下列问题: