题目内容
19.目前,产量最大,应用最广的金属是铁.图1所示是实验室里用一氧化碳还原氧化铁的实验装置,图2是炼铁高炉内发生的一连串化学反应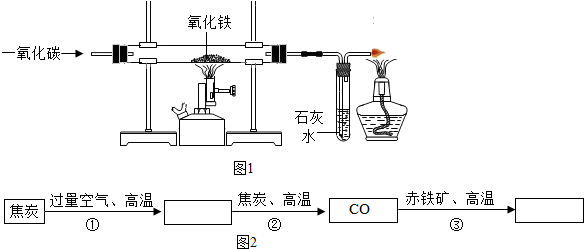
(1)图1中如果没有石灰水,能(填写“能”或“不能”)判断出一氧化碳已经和氧化铁反应,理由是玻璃管中的固体粉末由红色变成黑色.
(2)图2中第①步反应的产物是二氧化碳,写出步骤②的化学方程式C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO.
(3)根据图1实验可知,除一氧化碳具有还原性外,还可以得出一氧化碳的化学性质有可燃性,请写出相应的化学方程式2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
分析 (1)根据实验的生成物来分析;
(2)根据反应的过程及原理来分析;
(3)根据实验现象来分析.
解答 解:(1)在高温的条件下,一氧化碳能将红色氧化铁还原为黑色的铁,从而证明了反应的发生;故填:能;玻璃管中的固体粉末由红色变成黑色;
(2)碳在过量的氧气中充分燃烧生成二氧化碳;在高温的条件下,碳与二氧化碳反应生成一氧化碳;故填:二氧化碳;C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;
(3)尾气中含有一氧化碳,尾气能够燃烧说明一氧化碳具有可燃性,燃烧的生成二氧化碳.故填:可燃性;2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
点评 本题主要考查实验现象、化学方程式的书写等方面的知识,书写化学方程式时要遵循质量守恒定律.

练习册系列答案
相关题目
9.保护空气,使天空更蓝.下列做法合理的是( )
| A. | 使用绿色公共交通出行 | B. | 春节大量燃放鞭炮 | ||
| C. | 开发和利用石油 | D. | 将生活污水排放到江河中 |
7.大型综合交通枢纽-合肥南站,已开通运行,下列建设过程中涉及到化学变化的是( )
| A. |  规划设计 规划设计 | B. |  钢轨气焊 钢轨气焊 | ||
| C. |  安装座椅 安装座椅 | D. |  涂刷油漆 涂刷油漆 |
14.科学探究表明地球上水的状态除了气,液和固态外,还有玻璃态,玻璃态的水不存在晶体结构,密度与普通液态水相同,则下列说法正确的是( )
| A. | 玻璃态水不属于氧化物 | |
| B. | 玻璃态水分子不运动 | |
| C. | 玻璃态水和普通水的化学性质相同 | |
| D. | 玻璃态水分子间隔比普通水的分子间隔小 |
4.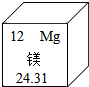 在元素周期表中,镁元素的某些信息如图所示,下列有关镁元素的说法中正确的是( )
在元素周期表中,镁元素的某些信息如图所示,下列有关镁元素的说法中正确的是( )
 在元素周期表中,镁元素的某些信息如图所示,下列有关镁元素的说法中正确的是( )
在元素周期表中,镁元素的某些信息如图所示,下列有关镁元素的说法中正确的是( )| A. | 原子序数为24.31 | B. | 属于非金属元素 | ||
| C. | 相对原子质量是24.31g | D. | 原子核外电子数为12 |
7.化学与生活、社会密切相关,下列说法正确的是( )
| A. | 食品添加剂有害人体健康,应禁止使用 | |
| B. | 购物时减少使用或不用塑料袋,是为了减少“白色污染” | |
| C. | 为防止土壤和水体富营养化,应禁止使用化肥与农药 | |
| D. | 不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质 |
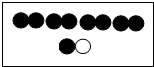
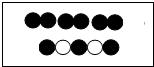
 甲、乙同学在学完酸的化学性质后,做了如图的实验:
甲、乙同学在学完酸的化学性质后,做了如图的实验: