题目内容
7. 如图是某硫酸试剂瓶标签上的部分文字说明.
如图是某硫酸试剂瓶标签上的部分文字说明.(1)取10mL该硫酸可配制成9.8%的硫酸180.32g.
(2)取适量9.8%的硫酸与某二价活泼金属112g反应可生成氢气4g,试通过计算确定该活泼金属的身份.
分析 溶液稀释前后溶质质量不变;
根据反应的化学方程式和提供的数据可以进行相关方面计算和判断.
解答 解:(1)设可配制成9.8%的硫酸质量为x,
根据题意有:1.84g/cm3×10mL×98%=x×10%,
x=180.32g,
故填:180.32.
(2)设金属的化学式为M,相对原子质量为x,
M+H2SO4═MSO4+H2↑,
x 2
112g 4g
$\frac{x}{112g}$=$\frac{2}{4g}$,
x=56,
铁的相对原子质量是56,因此该活泼金属是铁.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.物质的用途与性质密切相关.下列叙述错误的是( )
| A. | 因为氮气化学性质不活泼,所以可用于食品包装袋内防腐 | |
| B. | 因为活性炭具有吸附性,所以可利用活性炭将硬水转化为软水 | |
| C. | 因为镁能在空气中燃烧发出耀眼的白光,所以在军事上可以制作照明弹 | |
| D. | 因为“洗洁精”有乳化功能,所以“洗洁精”可用来洗涤餐具上的油污 |
12.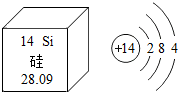 中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )
中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )
 中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )
中国科技大学熊宇杰教授课题组基于应用广泛的半导体硅材料,采用金属纳米结构的热电子注入方法,设计出一种可在近红外区域进行光电转换且具有力学柔性的太阳能电池.硅的原子结构示意图及它在元素周期表的某些信息如图所示,则下列说法正确的是( )| A. | 硅是金属元素 | B. | 硅的原子序数为28 | ||
| C. | 硅的相对原子质量为14 | D. | 硅的最外层电子数为4 |
13.“学做营养师,我来配食谱.”我帮小明完成下列食谱单.除水和无机盐外,下列食谱中,含有的营养素主要有糖类、油脂和蛋白质等;我认为小明的食谱中还缺乏一种人体必需的营养素,“我的补充”是水果
| 主食 | 米饭、馒头 |
| 副食 | 烧鱼块、咸鸭蛋、红烧肉、花生米 |
| 饮料 | 牛奶 |
| 我的补充 | ---- |