题目内容
某校课外活动小组的同学在测定由MgCl2和NaCl组成的固体混合物的组成时,进行了如下实验.取20克固体配成200克溶液,平均分成四份,然后分别加入一定质量分数的NaOH溶液,所得实验数据如表:
请分析数据,回答下列问题:
(1)m= ;
(2)20g原固体混合物溶液和足量NaOH溶液反应最多生成沉淀的质量 g;
(3)在实验三中,完全反应后所得溶液中氯化钠的质量分数是多少?(结果保留一位小数,写出计算过程) .
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 固体混合物溶液的质量/g | 50 | 50 | 50 | 50 |
| 加入NaOH溶液的质量/g | 10 | 20 | 30 | 40 |
| 生成沉淀的质量/g | 1 | m | 2.9 | 2.9 |
(1)m=
(2)20g原固体混合物溶液和足量NaOH溶液反应最多生成沉淀的质量
(3)在实验三中,完全反应后所得溶液中氯化钠的质量分数是多少?(结果保留一位小数,写出计算过程)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据加入10g氢氧化钠溶液质量得到沉淀1g,第三次实验加入30g氢氧化钠溶液生成沉淀增加了,说明第一次实验中10g氢氧化钠完全反应只能生成1g沉淀,加入20g氢氧化钠溶液质量是10g氢氧化钠溶液质量的2倍所以m值是1g的2倍;
(2)生成最多的沉淀的质量,应是完全反应后生成的沉淀质量,所以最多生成沉淀质量可由分析图表得到;
(3)根据反应的化学方程式,可以得到各物质之间的比例关系,进而求出生成的氯化钠的质量,再根据原固体混合物的质量减去氯化镁的质量求出原混合物中氯化钠的质量;完全反应后所得溶液中氯化钠的质量应是两者之和,进一步可求得完全反应后所得溶液中氯化钠的质量分数;
(2)生成最多的沉淀的质量,应是完全反应后生成的沉淀质量,所以最多生成沉淀质量可由分析图表得到;
(3)根据反应的化学方程式,可以得到各物质之间的比例关系,进而求出生成的氯化钠的质量,再根据原固体混合物的质量减去氯化镁的质量求出原混合物中氯化钠的质量;完全反应后所得溶液中氯化钠的质量应是两者之和,进一步可求得完全反应后所得溶液中氯化钠的质量分数;
解答:解:
(1)每加入10g氢氧化钠溶液质量得到沉淀1g,因此,第2次加入20g氢氧化钠溶液完全反应后,所得沉淀的总质量=1g×2=2g;
(2)根据图表可知,59g固体混合物中加入氢氧化钠溶液的质量到30g和40g时的沉淀质量一样多,说明加到30g 时已完全反应,故最多生成沉淀质量为2.9g,20g原固体混合物溶液和足量NaOH溶液反应最多生成沉淀的质量为
=1.16g
(3)设5g原固体混合物中氯化镁质量为x;生成氯化钠的质量为y
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 58 117
x 2.9g y
=
x=4.75g
=
y=5.85g
完全反应后所得溶液中氯化钠的质量为:(5g-4.75g)+5.85g=6.1g
完全反应后所得溶液中氯化钠的质量分数为:
×100%=7.9%
答案:
(1)2
(2)1.16g
(3)完全反应后所得溶液中氯化钠的质量分数为7.9%
(1)每加入10g氢氧化钠溶液质量得到沉淀1g,因此,第2次加入20g氢氧化钠溶液完全反应后,所得沉淀的总质量=1g×2=2g;
(2)根据图表可知,59g固体混合物中加入氢氧化钠溶液的质量到30g和40g时的沉淀质量一样多,说明加到30g 时已完全反应,故最多生成沉淀质量为2.9g,20g原固体混合物溶液和足量NaOH溶液反应最多生成沉淀的质量为
| 20g×2.9g |
| 50g |
(3)设5g原固体混合物中氯化镁质量为x;生成氯化钠的质量为y
MgCl2+2NaOH═Mg(OH)2↓+2NaCl
95 58 117
x 2.9g y
| 95 |
| 58 |
| x |
| 2.9g |
x=4.75g
| 58 |
| 2.9g |
| 117 |
| y |
y=5.85g
完全反应后所得溶液中氯化钠的质量为:(5g-4.75g)+5.85g=6.1g
完全反应后所得溶液中氯化钠的质量分数为:
| 6.1g |
| 50g+30g-2.9g |
答案:
(1)2
(2)1.16g
(3)完全反应后所得溶液中氯化钠的质量分数为7.9%
点评:此题是一道图表数据分析综合题,解题的关键是弄明白表格中数据的意义,进而判断出反应时的物质的质量情况,该题综合性较强,难度较大;

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
下列生产生活不涉及化学变化的是( )
| A、用大米发酵酿制白酒 |
| B、家里使用液化石油气煮饭 |
| C、用食盐来配制0.9%的生理盐水 |
| D、用稀盐酸除去菜刀上的铁锈 |
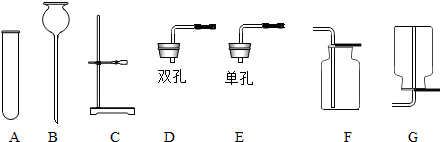
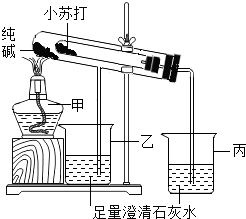 某化学兴趣小组设计了如图所示的装置,对纯碱(Na2CO3)和小苏打(NaHCO3)两种固体进行实验探究.
某化学兴趣小组设计了如图所示的装置,对纯碱(Na2CO3)和小苏打(NaHCO3)两种固体进行实验探究. 哈尔滨市春季平均气温低,为了使蔬菜提早上市,满足人们日常生活的需求.市政府扶持农民采用棚栽技术种植蔬菜,如图所示.请回答下列问题:蔬菜除了可以提供大量的水分外,提供的主要营养素对生命活动的主要作用是
哈尔滨市春季平均气温低,为了使蔬菜提早上市,满足人们日常生活的需求.市政府扶持农民采用棚栽技术种植蔬菜,如图所示.请回答下列问题:蔬菜除了可以提供大量的水分外,提供的主要营养素对生命活动的主要作用是