题目内容
19.21世纪是海洋开发与利用的世纪.烟台的“十二五”规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一.(1)海水淡化:蒸馏法淡化海水是利用海水中各成份的沸点不同分离出淡水;高压反渗透膜法淡化海水是利用海水中各成份的颗粒大小不同分离出淡水.
(2)制盐:①制粗盐.从卤水中提取粗盐用的结晶方法是蒸发结晶.②粗盐纯化.粗盐中含有泥沙、硫酸镁、氯化钙等杂质.将粗盐溶于水,然后通过如下操作即可得到较纯的氯化钠:a过滤.b加过量的Ba(OH)2溶液;c加适量的盐酸;d加过量的Na2CO3溶液;e蒸发.正确的操作顺序是bdace (填字母).
(3)制碱:氨碱法制纯碱的流程图如下:

完成图中的内容:①NH3;②CO2 ;③加热.
(4)制镁:工业上一般用电解熔融状态的氯化镁制金属镁,若以卤水(含有硫酸镁、氯化钠和氯化钙)为起始原料来制取金属镁,请画出制镁的流程图.
分析 (1)海水淡化的方法主要有:蒸馏法、结晶法、淡化膜法、多级闪急蒸馏法,可根据原理进行分析.
(2)①可根据氯化钠溶解度与温度的关系进行分析选择结晶方法.
②根据除杂时不引入新杂质的原理及实验目的进行分析.
(3)根据物质的化学性质进行选择试剂.
(4)可根据起始物质和最终物质进行正逆推导.
解答 解:(1)蒸馏法淡化海水是利用海水中各成份的沸点比较高,水的沸点比较低进行分离的;高压反渗透膜法淡化海水是利用海水中各成份的颗粒大小不同,水分子可以通过淡化膜,其它离子不会通过.
故答案为:沸点; 颗粒大小;
(2)因为氯化钠的溶解度随温度的变化不大,所以采用蒸发溶剂法结晶;
要除去粗盐中含有的杂质,可以加过量的氢氧化钡溶液除去硫酸镁,加过量的Na2CO3溶液除去氯化钙和过量试剂氢氧化钡,通过过滤把不溶于水的物质除去,加适量的盐酸除去过量的碳酸钠,通过蒸发除去盐酸.
故答案为:蒸发结晶;bdace;
(3)根据题中所给生成物进行分析,要制备饱和氨水肯定是将氨水通入食盐水中,由饱和的氨水食盐溶液制备碳酸氢钠,根据物质的性质和元素守恒知应通入二氧化碳气体;碳酸氢钠受热易分解变为碳酸钠.
故答案为:①NH3 ②CO2 ③加热;
(4)首先必须将卤水中镁进行富集,加入石灰乳(比较经济,不能用氢氧化钠),变为氢氧化镁沉淀,过滤后加入盐酸制备氯化镁,再经过蒸发干燥制备无水氯化镁,最后经过通电可制得镁.
故答案为:卤水$\stackrel{石灰乳}{→}$$\stackrel{过滤}{→}$ 氢氧化镁$\stackrel{盐酸}{→}$氯化镁溶液$\stackrel{蒸发溶剂}{→}$$\stackrel{干燥}{→}$无水氯化镁$\stackrel{通电}{→}$镁
点评 本题难度比较大,涉及海水淡化方法的原理、海水晒盐的原理、除杂的原理、侯氏制碱法的原理等理论内容,要通过该题认真总结.

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案| A. | 一氧化碳、二氧化碳和氢氧化钙都含有氧元素,它们都属于氧化物 | |
| B. | 氨水(NH3.H2O)是一种碱,纯碱是一种盐 | |
| C. | 铜锈的主要成分的化学式为Cu2(OH)2CO3,铜锈是一种盐也是一种碱 | |
| D. | 不含结晶水的晶体是纯净物,含结晶水的晶体是混合物 |
| A. |  由实验可以得出水是由氢气和氧气组成的 | |
| B. | 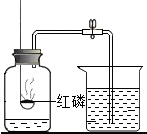 当装置漏气时,测得的空气中氧气体积分数偏大 | |
| C. |  该装置实验可以说明燃烧的条件之一是温度需达到可燃物的着火点 | |
| D. |  用装置收集氧气,气体要从a端进入 |
| A. | H2 | B. | H2O | C. | 2H | D. | H |
(1)在该探究实验中,同学们将车流量设置为实验的变量,根据表中数据可以得出,在市区的A地段,空气中PM2.5的浓度在下班时段最大.
| 组别 | PM2.5(微克/立方米) | |||
| 清晨 (车流量最小) | 上班时段 (车流量大) | 中午 (车流量小) | 下班时段 (车流量最大) | |
| 第1组 | 19 | 89 | 43 | 97 |
| 第2组 | 22 | 83 | 38 | 98 |
| 第3组 | 20 | 86 | 41 | 99 |
(3)下列措施中,有利于减少雾霾天气发生的是ABD.
A.增加绿化面积 B.过年时少放或不放烟花爆竹
C.提倡秸秆焚烧 D.减少汽车的使用,近距离提倡自行车出行
(4)为了降低汽车排放的尾气对空气的污染,现在的大部分汽车都安装了催化式排气净化器.如CO和NO在催化剂的作用下会生成N2和CO2,请写出该反应化学方程式:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.
| A. | 氟 | B. | 氯 | C. | 溴 | D. | 碘 |