题目内容
下列说法中正确的是( )
| A、根据质量守恒定律,10g食盐溶于90g水中,得溶液质量是100g |
| B、根据质量守恒定律,2L氢气与1L氧气恰好完全反应,生成3L水 |
| C、根据质量守恒定律,12gC在10gO2中充分燃烧,生成22gCO2 |
| D、根据质量守恒定律,蜡烛燃烧后生成物的质量之和等于蜡烛减少的质量与消耗氧气的质量之和 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:质量守恒定律是指在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.据此进行分析选择.
解答:解:
A、10g食盐溶于90g水中是物理变化,不是化学变化,所以不能用质量守恒定律来解释.故A不适合;
B、质量守恒定律是指质量守恒,而非体积守恒.故B不适合;
C、12g碳与32g氧气恰好完全反应可生成44g二氧化碳.生成物质量=反应物质量之和,而“12gC在10gO2中”,不能充分燃烧,生成CO2小于22g.故C适合;
D、根据质量守恒定律,蜡烛燃烧后生成物的质量之和等于蜡烛减少的质量与消耗氧气的质量之和.
故选D.
A、10g食盐溶于90g水中是物理变化,不是化学变化,所以不能用质量守恒定律来解释.故A不适合;
B、质量守恒定律是指质量守恒,而非体积守恒.故B不适合;
C、12g碳与32g氧气恰好完全反应可生成44g二氧化碳.生成物质量=反应物质量之和,而“12gC在10gO2中”,不能充分燃烧,生成CO2小于22g.故C适合;
D、根据质量守恒定律,蜡烛燃烧后生成物的质量之和等于蜡烛减少的质量与消耗氧气的质量之和.
故选D.
点评:本题主要考查学生运用质量守恒定律以及物理变化和化学变化的特征进行分析推断的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
生活中处处离不开化学知识,下列说法中,错误的是( )
| A、煲骨头汤时放点醋能更好的帮助补钙 |
| B、pH<5.6的雨水称为酸雨 |
| C、为使发面食品口感好,制作时可添加适量纯碱 |
| D、“温室效应”主要是由CO等气体引起的 |
下列粒子结构示意图中,表示阳离子的是( )
A、 |
B、 |
C、 |
D、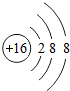 |
下列结构示意图表示的微粒中,最易得到电子的是( )
A、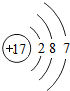 |
B、 |
C、 |
D、 |
下列实验现象描述与事实不符合的是( )
| A、水通电一段时间后,得到的氧气与氢气在相同条件下体积比约为1:2 |
| B、木炭在氧气中燃烧,发出白光,生成一种使澄清石灰水变浑浊的气体 |
| C、镁与稀盐酸反应产生气泡,溶液由无色变成浅绿色 |
| D、氢气燃烧发出淡蓝色火焰,放出大量的热 |
下列有关实验操作中“量”的说法错误的是( )
| A、实验中没有规定取用药品的量时,可以按任意量取用 | ||
B、给试管中的液体加热,液体的量不能超过试管容积的
| ||
C、酒精灯内的酒精量最多不超过酒精灯容积的
| ||
D、洗涤试管时,可注入
|
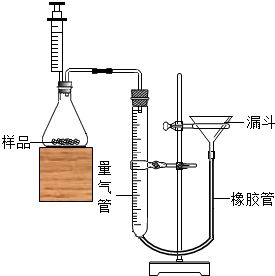 为了测定某铜锌合金的组成,校化学课外活动小组设计了如图所示的实验装置进行实验.
为了测定某铜锌合金的组成,校化学课外活动小组设计了如图所示的实验装置进行实验.