题目内容
14.下列离子能在pH=13的无色溶液中大量共存的是( )| A. | K+、OH-、SO42-、Cu2+ | B. | CO32-、K+、Cl-、Ca2+ | ||
| C. | H+、Ba2+、Cl-、NO3- | D. | K+、NO3-、Na+、OH- |
分析 根据pH为13的水溶液显碱性,水溶液中含有大量的OH-.根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存,且注意带色的物质,据此进行分析判断即可.
解答 解:pH为13的水溶液显碱性,水溶液中含有大量的OH-.
A、铜离子和碱性溶液中的中OH-在溶液中结合生成氢氧化铜沉淀,不能大量共存,且铜离子显蓝色,故选项错误;
B、碳酸根离子和钙离子会生成碳酸钙沉淀,不能共存,故选项错误;
C、氢离子和碱性溶液中的中OH-在溶液中结合生成水,不能大量共存,故选项错误;
D、三种物质在碱性溶液中相互交换成分不能生成沉淀、气体、水,能在溶液中大量共存,且不存在带色的离子,故选项正确;
故选D.
点评 本题考查了常见离子的共存问题,完成此题,可以依据复分解反应的实质进行,要求同学们熟记常见的酸碱盐在水中的溶解性,以便灵活应用.

练习册系列答案
相关题目
4.四氧化三铁可用于医疗器械、电子等工业.某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表所示.
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液.
(3)制备Fe3O4的实验流程如下:
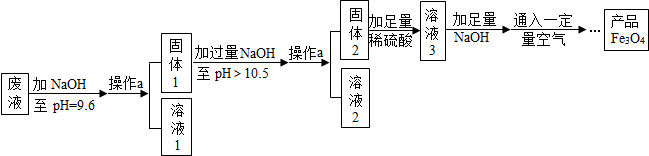
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4(写出其中一个).
(2)操作a的名称为过滤.该操作需要的玻璃仪器有烧杯、玻璃棒、漏斗等.玻璃棒在此操作中的主要作用是引流.
(3)溶液1所含溶质有NaOH、Na2SO4、MgSO4(至少写两种成分的化学式);溶液3所含溶质的主要成分为硫酸亚铁(写名称).
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表所示.
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(3)制备Fe3O4的实验流程如下:

【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4(写出其中一个).
(2)操作a的名称为过滤.该操作需要的玻璃仪器有烧杯、玻璃棒、漏斗等.玻璃棒在此操作中的主要作用是引流.
(3)溶液1所含溶质有NaOH、Na2SO4、MgSO4(至少写两种成分的化学式);溶液3所含溶质的主要成分为硫酸亚铁(写名称).
9.“西气东输”工程输送气体的主要成分是( )
| A. | 甲烷 | B. | 一氧化碳 | C. | 氢气 | D. | 氧气 |
19.照相馆废弃的定影液含有银.回收方法是Fe+2AgNO3=2Ag+Fe(NO3)2,该反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
3.现将X、Y两种金属片分别插入硫酸铜溶液中,X无明显变化,Y表面有铜析出,则X、Y、Cu三种金属的活动性由强到弱的顺序是( )
| A. | X>Y>Cu | B. | Cu>X>Y | C. | X>Cu>Y | D. | Y>Cu>X |
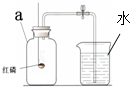 如图是小张同学测定空气中氧气体积分数的实验装置,根据题意回答以下问题.
如图是小张同学测定空气中氧气体积分数的实验装置,根据题意回答以下问题.