题目内容
一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量(g) | 1 | 30 | 17 | 2 |
反应后质量(g) | m | 39 | 0 | 10 |
关于此反应,下列认识不正确的是
A.表中m为1g B.甲可能是该反应的催化剂
C.该反应是化合反应 D.反应中乙、丁的质量比为9:8
C
【解析】根据质量守恒定律,由表格信息可知反应后乙、丁的质量分别增加了9g、8g,是生成物;丙的质量减少了17g,是反应物;因为反应物的质量总和=9g+8g=17g,与生成丙的质量相等,所以甲的质量不变,则m值是1g,可能是该反应的催化剂;该反应由一种物质生成两种物质,属于分解反应;乙与丁的质量之比为9:8,所以A、B、D正确,不符合题意,C错误, 符合题意.故选C.
试题分析:根据表格中的数据分析,反应前后质量增加的是生成物,减少的是反应物,质量不变的可能是催化剂或杂质,结合质量守恒定律推断m值;计算乙、丁的质量比;根据化合反应是多种物质生成一种物质的反应,结合题意中的反应物和生成物分析;根据催化剂的特点和甲物质在反应前后的质量变化分析.
考点:质量守恒定律的含义及应用

练习册系列答案
相关题目



 .H
.H O)的药水,可减轻痛痒,NH
O)的药水,可减轻痛痒,NH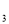 .H
.H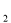 O中的氮元素的化合价为
O中的氮元素的化合价为