题目内容
有含两种金属的合金11.2克与足量的稀盐酸充分反应后生成氢气的质量为0.4克,则该合金含的金属可能是( )
| A、Al、Mg |
| B、Mg、Fe |
| C、Fe、Zn |
| D、Mg、Zn、 |
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:利用一定质量金属完全反应放出氢气质量=
×金属质量,计算生0.4g氢气消耗选项所涉及金属铁、锌、镁、铝的质量;然后根据题设的条件:两种金属混合物11.2g,与足量稀盐酸反应后生成0.4g氢气,推断出两种金属混合物的可能组成.
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:根据与硫酸反应时铁、锌、镁、铝分别呈+2、+2、+2、+3,与足量稀硫酸反应后生成了0.4g氢气,所需要消耗金属的质量分别为:
需要金属铁的质量=0.4g×
=11.2g;需要金属锌的质量0.4g×
=32.5g;需要金属镁的质量=0.4g×
=4.8g;需要金属铝的质量=0.4g×
=3.6g;根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中两种金属混合物11.2g与足量稀盐酸反应后生成了0.4g氢气,可判断选项混合物中两种金属只可能为镁和锌、铝和锌的混合物.
故选项为:D.
需要金属铁的质量=0.4g×
| 56 |
| 2 |
| 65 |
| 2 |
| 24 |
| 2 |
| 27 |
| 3 |
故选项为:D.
点评:本题考查了金属与酸反应产生氢气的关系的计算,依据常见的总结公式一定质量金属完全反应放出氢气质量═
×金属质量进行计算或利用化学方程式进行计算或利用平均相对原子质量计算均可,需要注意到铁在与酸发生置换反应时呈现出+2价.
| 金属的化合价 |
| 金属的相对原子质量 |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
物质发生化学反应前后,一定不发生变化的是( )
①物质的质量总和 ②物质的种类 ③元素的种类 ④原子的数目
⑤原子的种类 ⑥物质的分子总数 ⑦原子的质量 ⑧物质的性质.
①物质的质量总和 ②物质的种类 ③元素的种类 ④原子的数目
⑤原子的种类 ⑥物质的分子总数 ⑦原子的质量 ⑧物质的性质.
| A、全部 | B、①②③④⑤⑥⑦ |
| C、①③⑤ | D、①③④⑤⑦ |
已知在CO和CO2的混合气体中,碳元素和氧元素的质量比为1:2,则CO和CO2的质量比为( )
| A、2:1 | B、7:11 |
| C、11:7 | D、7:8 |
关于元素周期表的叙述错误的是( )
| A、元素周期表共有7个周期 |
| B、元素周期表中共有18个纵行,即18个族 |
| C、它是学习和研究化学知识的重要工具 |
| D、它是俄国化学家门捷列夫发现的 |
下列有关分子和原子的说法不正确的是( )
| A、分子、原子都是构成物质的基本粒子 |
| B、分子、原子的质量和体积都很小 |
| C、分子、原子总在不断运动 |
| D、分子之间有间隔,原子之间没有间隔 |
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、O3、ClO2氧化性更强,且没有二次污染.高铁酸钾与水反应的化学方程式是:4K2FeO4+10H2O═4X↓+8KOH+3O2↑.以下有关高铁酸钾的说法不正确的是( )
| A、高铁酸钾属于氧化物 |
| B、高铁酸钾应密封、防水保存 |
| C、高铁酸钾中铁显+6价 |
| D、X的化学式是Fe(OH)2 |
下列说法正确的是( )
| A、煤气可作为生活燃气,其成分为CO |
| B、水基型灭火器灭火时利用泡沫带出二氧化碳附着在可燃物表面,使其与氧气隔绝 |
| C、“低碳”是指较低碳单质的利用与排放 |
| D、在工业上,采用物理或化学方法人工吸收二氧化碳,可以控制二氧化碳的排放量 |
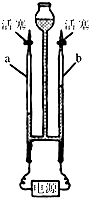 (1)科学家用通电的方法使水分解,从而证明了水的组成.把水注入水电解器装置甲中,接通直流电,可以观察到a管中的电极上
(1)科学家用通电的方法使水分解,从而证明了水的组成.把水注入水电解器装置甲中,接通直流电,可以观察到a管中的电极上 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.