题目内容
20. 铝元素与人类关系密切
铝元素与人类关系密切(1)铝是地壳中含量最高的金属元素.
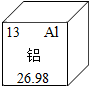
(2)元素周期表中铝元素的信息如图所示,其原子的核外电子数为13.
(3)铝元素在自然界中主要以Al2O3存在,Al2O3属于B(填字母序号)
A.单质 B.氧化物 C.碱 D.盐
(4)铝可制成蒸锅,主要利用铝的延展性和导热性.
(5)药品“氢氧化铝[Al(OH)3]”能与胃酸(主要成分为盐酸)发生中和反应治疗胃酸过多症,该反应的化学方程式为Al(OH)3+3HCl═AlCl3+3H2O;.
(6)铝具有很好的抗腐蚀性能,是因为铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜,其反应的化学方程式是4Al+3O2=2Al2O3.
分析 (1)据地壳中元素的含量分析;
(2)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数,汉字下面的数字表示相对原子质量,进行分析解答即可.
(3)根据氧化物的概念进行分析解答.
(4)根据金属具有良好的导电性、导热性、延展性,结合用途进行分析解答即可;
(5))依据原理找出反应物、生成物和反应条件,根据方程式的书写规则书写方程式;
(6)根据铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜分析.
解答 解:(1)地壳中元素的含量由多到少的顺序是:氧、硅、铝、铁、钙,铝是地壳中含量最高的 金属元素;
(2)根据元素周期表中的一格可知,左上角的数字为13,表示原子序数为13;根据原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为13.
(3)由两种元素组成,其中一种为氧元素的化合物为氧化物,故Al2O3属于氧化物.
(4)铝可制成蒸锅,主要利用铝的延展性和导热性.
(5)反应物为氢氧化铝和盐酸,生成物为氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O;
(6)铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜,因此铝具有很好的抗腐蚀性能,化学方程式为:4Al+3O2=2Al2O3;
故答案为:(1)金属(2)13;(3)B;(4)导热(5)Al(OH)3+3HCl═AlCl3+3H2O;(6)铝能够被空气中的氧气氧化,从而在铝表面形成一层保护膜;4Al+3O2=2Al2O3
点评 本题难度不大,掌握元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、四种基本反应类型的特征、金属的物理性质与用途是正确解答本题的关键.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
11.我国大部分地区深受酸雨的危害,煤燃烧产生的SO2是形成酸雨的主要污染物,SO2与水结合生成弱酸性亚硫酸(H2SO3).
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色.
(1)酸雨是pH小于5.6的降雨.
(2)常用脱硫方法减少废气中的SO2,以生石灰(CaO)为脱硫剂,高温下与废气中的SO2
与O2化合生成CaSO4,化学方程式为2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4
(3)实验室常用亚硫酸盐与HCl或H2SO4反应制备SO2,Na2SO3与盐酸发生反应的基本类型为Na2SO3+2HCl═2NaCl+H2O+SO2↑
(4)小明同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足
量的NaOH,并就反应后混合溶液的中盐成分进行如下探究:
[提出问题]反应后的混合溶液中盐的成份是什么?
[进行猜想]猜想1:只有Na2SO3
猜想2:只有Na2SO4
猜想3:既有Na2SO4,也有Na2SO3
[实验探究]限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液
已知:H2SO3易分解生成水和SO2,也易与空气中的氧气或稀硝酸反应生成H2SO4;H2SO3和SO2都能使红色的品红溶液褪色.
(1)酸雨是pH小于5.6的降雨.
(2)常用脱硫方法减少废气中的SO2,以生石灰(CaO)为脱硫剂,高温下与废气中的SO2
与O2化合生成CaSO4,化学方程式为2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4
(3)实验室常用亚硫酸盐与HCl或H2SO4反应制备SO2,Na2SO3与盐酸发生反应的基本类型为Na2SO3+2HCl═2NaCl+H2O+SO2↑
(4)小明同学利用中和反应的原理,在空气中放置一段时间的酸雨(pH约为3)中加入足
量的NaOH,并就反应后混合溶液的中盐成分进行如下探究:
[提出问题]反应后的混合溶液中盐的成份是什么?
[进行猜想]猜想1:只有Na2SO3
猜想2:只有Na2SO4
猜想3:既有Na2SO4,也有Na2SO3
[实验探究]限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、澄清石灰水、品红溶液、紫色石蕊溶液
| 步骤 | 实验操作 | 预期现象和结论 |
| 1 | 各取2mL反应后的混合溶液分别加入A、B两只试管中 | 多余空 |
2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | 有气泡产生,品红溶液褪色,证明含有Na2SO3 |
3 | 向B试管中,加入足量的氯化钡溶液溶液,再加入足量的稀盐酸 | 先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有Na2SO4,则猜想3成立 |
8.逻辑推理是化学学习常用的思维方法.下列观点正确的是( )
| A. | 酸的溶液pH值小于7,碱的溶液pH大于7,所以盐的溶液pH值一定等于7 | |
| B. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 | |
| C. | 氧化物只含有两种元素,所以氧化物中一定有一种元素不是氧元素 | |
| D. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
15.下列推理合理的是( )
| A. | 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| B. | CO2能灭火,既利用了CO2的物理性质又利用了CO2的化学性质 | |
| C. | 碱溶液能使酚酞变红,所以能使酚酞变红的试液一定是碱溶液 | |
| D. | 酸性溶液的pH<7,所以pH<7的雨水是酸雨 |
5.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,向烧杯中的氢氧化钙溶液中滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中溶质的成分进行研究.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】(A)溶质可能是CaCl2与Ca(OH)2 (B)溶质可能是CaCl2 (C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写表格:
通过以上探究,最后确定猜想(C)正确.
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀铁质下水道
水污染,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的石灰石,充分反应后过滤,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】(A)溶质可能是CaCl2与Ca(OH)2 (B)溶质可能是CaCl2 (C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液与试管中,逐滴加入碳酸钠溶液 | 产生沉淀 | 猜想(B)正确 |
| 先产生气泡,后产生沉淀 | 猜想(C)正确 |
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀铁质下水道
水污染,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的石灰石,充分反应后过滤,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
12.食品卫生与身体健康密切相关,下列做法会导致食品对人体有害的是( )
①用加入三聚氰胺来提高奶粉的含氮量
②用福尔马林(甲醛的水溶液)浸泡海鲜产品来保鲜
③用小苏打(碳酸氢钠)发面做馒头使其松软可口
④用硫磺熏制生姜或种植时使用农药神农丹.
①用加入三聚氰胺来提高奶粉的含氮量
②用福尔马林(甲醛的水溶液)浸泡海鲜产品来保鲜
③用小苏打(碳酸氢钠)发面做馒头使其松软可口
④用硫磺熏制生姜或种植时使用农药神农丹.
| A. | ①③ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
9.小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究.
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有A.
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液 )
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH;④…..
【实验验证】(提示CaCl2溶液显中性)
【反思评价】有同学提出将CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立.小刚同学认为不正确,其理由是:无法确定溶液中是否存在氢氧化钠.
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有A.
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液 )
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH;④…..
【实验验证】(提示CaCl2溶液显中性)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 有白色沉淀产生 溶液仍为红色 | 猜想③成立 |
10.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下,则下列说法正确的是( ) 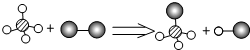
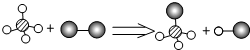
| A. | 反应物都是单质,生成物都是化合物 | |
| B. | 该化学变化还随着能量变化 | |
| C. | 该反应属于置换反应 | |
| D. | 该反应不符合质量守恒定律 |