题目内容
某化合物完全燃烧,需要9.6g氧气,同时生成8.8gCO2和5.4g水,则此化合物中( )
| A、一定含有氧元素 |
| B、一定含有碳元素和氢元素,可能含有氧元素 |
| C、一定不含有氧元素 |
| D、只含有碳、氢两种元素 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.
解答:解:8.8克二氧化碳中,氧元素的质量为:8.8克×
×100%=6.4g;
5.4克水中,氧元素的质量为:5.4克×
×100%=4.8g;
二氧化碳和水中,氧元素的质量和为:6.4g+4.8g=11.2g;
由以上计算可知,该化合物中含有碳元素、氢元素和氧元素;
故选A.
| 32 |
| 44 |
5.4克水中,氧元素的质量为:5.4克×
| 16 |
| 18 |
二氧化碳和水中,氧元素的质量和为:6.4g+4.8g=11.2g;
由以上计算可知,该化合物中含有碳元素、氢元素和氧元素;
故选A.
点评:在化学反应中遵循质量守恒定律,参加反应的物质的质量总和等于反应后生成的物质的质量总和.

练习册系列答案
相关题目
化学学习小组复习元素及其化合物知识以后,交流自己的学习体会,以下是四位同学的发言,其中有错误的是( )
| A、碳能形成多种单质,如:金刚石、石墨、C60等.碳具有还原性,用焦炭可冶炼铁 |
| B、SO3、CO2、CO是非金属氧化物,都可用NaOH溶液吸收 |
| C、铁是化学性质比较活泼的金属,除与氧气反应外,还能与某些酸和盐溶液发生置换反应 |
| D、C、CO、CH4、C2H5OH均能作为燃料使用 |
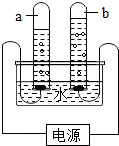 如图表示通电分解水的简易装置.回答下列问题:
如图表示通电分解水的简易装置.回答下列问题:(1)与a试管中的电极相连接的是电池
(2)如果该实验中,b试管中产生气体质量的为32g,则a试管中产生气体的质量为
(3)该实验得出的结论是:
某不纯的硝酸铵(NH4NO3)样品中,含98%的硝酸铵(杂质不含氮),则样品中的氮元素的质量分数是( )
| A、35% | B、35.7% |
| C、34.3% | D、17.15% |
化学反应前后肯定发生变化的是( )
| A、原子数目 | B、元素种类 |
| C、物质总质量 | D、分子种类 |
下列物质中属于纯净物的是( )
| A、生理盐水 | B、消毒酒精 |
| C、碘酒 | D、冰水混合物 |
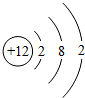 ,镁原子在化学反应中容易
,镁原子在化学反应中容易