题目内容
8.写出或配平化学方程式(1)硫磺在空气中燃烧S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
(2)配平:①□C6H6+□O2═□CO2+□H2O,配平后的系数从左到右依次为2、15、12、6
(3)过氧化钠是一种淡黄色粉末,在常温情况下能跟二氧化碳反应生成碳酸钠和氧气.写出化学方程式:2Na2O2+2CO2═2Na2CO3+O2.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法(最小公倍数法、定一法等)进行配平即可;配平时要注意化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整数.
解答 解:(1)硫磺在空气中燃烧生成二氧化硫,反应的化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.
(2)本题可利用“定一法”进行配平,把C6H6的化学计量数定为1,则O2、CO2、H2O前面的化学计量数分别为:$\frac{15}{2}$、6、3,同时扩大2倍,则C6H6、O2、CO2、H2O前面的化学计量数分别为2、15、12、6.
(3)过氧化钠在常温情况下能跟二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.
故答案为:(1)S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;(2)2、15、12、6;(3)2Na2O2+2CO2═2Na2CO3+O2.
点评 本题难度不大,掌握化学方程式的书写方法、配平方法等是正确解答本题的关键.

练习册系列答案
相关题目
3.下列化学方程式、实验现象或用途都正确的是( )
| A. | S+O2═SO2在纯氧中燃烧,发出淡蓝色火焰 | |
| B. | 3H2SO4+2Fe═Fe2(SO4)3+3H2O 铁钉逐渐溶解,溶液由无色变成黄色 | |
| C. | Ca(OH)2+Na2CO3═CaCO3↓+NaOH 可用于工业上制备烧碱 | |
| D. | NaCl+AgNO3═AgCl↓+NaNO3可用于检验汗液中是否含有Cl- |
20.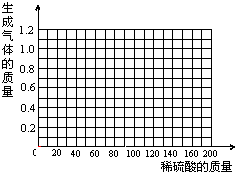 黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
按要求回答下列问题:
(1)根据实验数据分析,从第4份开始,金属已经反应完全了.
(2)列式计算该黄铜样品中金属锌的质量分数.(要求写出计算过程)
(3)列式计算稀硫酸的溶质质量分数.(要求写出计算过程)
(4)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线.
 黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品.为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:| 样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
| 取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
| 取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
| 产生气体质量(g) | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
(1)根据实验数据分析,从第4份开始,金属已经反应完全了.
(2)列式计算该黄铜样品中金属锌的质量分数.(要求写出计算过程)
(3)列式计算稀硫酸的溶质质量分数.(要求写出计算过程)
(4)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线.
17.如图所示的基本实验操作中错误的是( )
| A. | 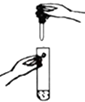 滴加少量液体 | B. | 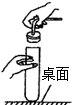 塞紧橡皮塞 | C. | 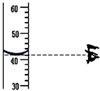 读取液体体积 | D. |  闻气体气味 |
18.关于分子、原子的叙述不正确的是( )
| A. | 化学反应中的原子不能再分成更小的粒子 | |
| B. | 物质都是由原子、分子等微小粒子构成的 | |
| C. | 在化学变化中分子分成原子,原子又重新组合成新的分子 | |
| D. | 分子是保持物质化学性质的最小粒子,也是化学变化中的最小粒子 |