题目内容
6.等质量的下列物质在氧气中充分燃烧,消耗氧气的物质的量最多的是( )| A. | 镁 | B. | 铁 | C. | 硫 | D. | 碳 |
分析 根据化学方程式可以计算出消耗氧气的质量,然后进行比较即可得出本题答案.
解答 解:通过分析题可知,写出四种物质的反应化学方程式,写出各物质之间的反应关系,设参加反应的各物质的质量为a,
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,
48 32
a $\frac{2a}{3}$
C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2,
12 32
a $\frac{8a}{3}$
S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2,
32 32
a a
3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,
168 64
a $\frac{8a}{21}$
通过分析可知,等质量的物质在氧气中充分燃烧,消耗氧气质量最多的是碳,而氧气的物质的量是氧气质量和摩尔质量的比值,所以碳消耗的氧气的物质的量最大,
故选:D.
点评 本题主要考查了化学方程式的计算,难度不大,注意正确写出化学方程式即可解答.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
16.常温下,下列各组物质中,X既能与Y反应又能与Z反应的是( )
| 选项 | X | Y | Z |
| A | CO2 | Ca(OH)2溶液 | H2O |
| B | Ba(NO3)2溶液 | 稀硫酸 | Na2CO3溶液 |
| C | Al | O2 | Mg(NO3)2 |
| D | Fe2O3 | 稀盐酸 | CO |
| A. | A | B. | B | C. | C | D. | D |
14.补铁酱油、高钙奶粉中的“铁”“钙”指的是( )
| A. | 单质 | B. | 元素 | C. | 原子 | D. | 分子 |
11.DHA被称为脑黄金,对婴儿智力和视力发育至关重要,其化学式是C22H32O2,下列说法不正确的是( )
| A. | DHA属于有机化合物 | |
| B. | DHA分子中碳、氢、氧元素质量比为11:16:1 | |
| C. | 每一个DHA分子由56原子构成 | |
| D. | DHA中碳元素质量分数最高 |
18.下列基本实验操作正确的是( )
| A. | 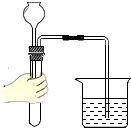 检查气密性 检查气密性 | B. |  闻药品的气味 | C. | 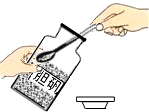 取固体药品 | D. | 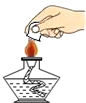 熄灭酒精灯 |
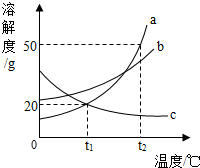 如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题:
如图是a、b、c三种固体物质的溶解度曲线,请回答下列问题: