题目内容
9.化学帮助我们认识身边的物质①引起酸雨的主要物质是SO2;
②引起温室效应的物质是CO2;
③草木灰主要成分的化学式是K2CO3;
④用来中和酸性土壤的碱是氢氧化钙;;
⑤碳具还原性可以冶炼金属,写出碳和氧化铜反应的化学方程式C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
⑥麻黄碱(C10H15ON)可用于治疗支气管哮喘.C10H15ON由4种元素组成,其摩尔质量是_165g/mol,1mol C10H15ON中约含有6.02×1024个C原子(用科学记数法表示).
分析 ①根据二氧化硫能与水反应生成酸解答;
②引起温室效应的物质是二氧化碳解答;
③根据草木灰的主要成分是碳酸钾解答;
④根据用来中和酸性土壤的碱是氢氧化钙解答;
⑤根据碳和氧化铜反应生成铜和二氧化碳,写出反应的化学方程式解答;
⑥据麻黄碱(C10H15ON)可知醋酸由C、H、O、N四种元素组成,根据标在元素符号右下角的数字表示一个分子中所含原子的个数进行解答;根据“每1摩尔任何物质含有阿伏伽德罗常数(约6.02×1023)个微粒”进行解答.
解答 解:
①二氧化硫能与雨水反应生成酸,导致雨水的pH小于5.6而成为酸雨;故答案为:SO2;
②引起温室效应的物质是二氧化碳;
③草木灰的主要成分是碳酸钾,化学式为:K2CO3;
④用来中和酸性土壤的碱是氢氧化钙;
⑤碳和氧化铜反应生成铜和二氧化碳,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
⑥根据麻黄碱(C10H15ON)可知醋酸由C、H、O、N四种元素组成;其摩尔质量是12×10+1×15+16+14=165g/mol,1mol C10H15ON中约含有10×6.02×1023=6.02×1024;
答案:
①SO2;
②CO2
③K2CO3;
④氢氧化钙;
⑤C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
⑥4;165;6.02×1024;
点评 本题考查了与我们密切相关的空气、水、二氧化碳和醋酸的相关知识.明克化学式的意义及根据化学式确定组成物质元素之间的质量关系是解答本题的关键.

练习册系列答案
相关题目
19.实验室制取二氧化碳并验证其性质的实验装置如图所示,其叙述正确的是( )


| A. | ①所示仪器甲是长颈漏斗 | B. | ④说明CO2能使石蕊试液变红 | ||
| C. | ③可用于收集和检验气体 | D. | ④⑤⑥只能验证其化学性质 |
20.以下初中阶段所学的相关化学知识、说法以及解释,其中正确的是( )
| 相关化学知识、说法 | 解释 | |
| A | 碳、硫与氧气反应是化合反应 | 氧气均支持这些物质燃烧 |
| B | 氧化钙和浓硫酸加入水都放热 | 二者均发生了化学变化 |
| C | 稀硫酸、硫酸铜溶液显酸性 | 溶液中均含有硫酸酸根离子 |
| D | 乙醇和甲烷都是有机物 | 二者均为碳元素的化合物 |
| A. | A | B. | B | C. | C | D. | D |
17.属于化学变化的是( )
| A. | 纸张燃烧 | B. | 花香四溢 | C. | 灯泡发光 | D. | 滴水成冰 |
4.实验操作正确的是( )
| A. |  | B. | 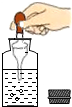 | C. | 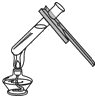 | D. |  |
1.为了测定某铜锌混合物中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
①每一次反应中生成氢气的物质的量是0.2mol.
②试计算该铜锌合金中锌的质量分数(写出计算过程).52%
③从上表数据分析,当所取合金与所用稀硫酸的质量比为1:4时,表明合金中的锌与稀硫酸中的硫酸恰好完全反应.
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀硫酸的质量/g | 120 | 160 | 100 |
| 生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
②试计算该铜锌合金中锌的质量分数(写出计算过程).52%
③从上表数据分析,当所取合金与所用稀硫酸的质量比为1:4时,表明合金中的锌与稀硫酸中的硫酸恰好完全反应.
18. 铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )
铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )
 铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )
铬是重要的合金元素,镀在金属上可以防锈,元素周期表中“铬”的信息如图所示,下列关于铬元素说法正确的是( )| A. | 是非金属元素 | B. | 原子序数为24 | ||
| C. | 相对原子质量为52.00g | D. | 中子数为24 |
 NaCl、KN03两种物质的溶液度曲线图如图所示,请回答:
NaCl、KN03两种物质的溶液度曲线图如图所示,请回答: 小然同学设计探究分子运动的实验如图,请按要求完成下列各小题:
小然同学设计探究分子运动的实验如图,请按要求完成下列各小题: