题目内容
CO和CO2的混合气体10克,通过炽热的足量氧化铜粉末,生成了6.4克红色的铜.问:参加反应的一氧化碳的质量是多少?混合气体中二氧化碳的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据已知量6.4g金属铜,设出一氧化碳的质量,根据CO+CuO
Cu+CO2,求出一氧化碳的质量,再求出二氧化碳的质量,
| ||
解答:解:设混合气体中CO的质量为x
CO+CuO
Cu+CO2
28 64
x 6.4g
=
x=2.8g
所以二氧化碳的质量为 10g-2.8g=7.2g
混合气体中二氧化碳的质量分数是
×100%=72%
答案:参加反应的一氧化碳的质量是2.8g,混合气体中二氧化碳的质量分数是72%.
CO+CuO
| ||
28 64
x 6.4g
| 28 |
| x |
| 64 |
| 6.4g |
x=2.8g
所以二氧化碳的质量为 10g-2.8g=7.2g
混合气体中二氧化碳的质量分数是
| 7.2g |
| 10g |
答案:参加反应的一氧化碳的质量是2.8g,混合气体中二氧化碳的质量分数是72%.
点评:在解此类题时,首先分析题中的反应原理,然后结合题中方程式中的等量关系进行分析解答需要的数据,再结合题意进行计算.

练习册系列答案
相关题目
14g某物质完全燃烧,只生成44gCO2和18gH2O,则该物质可能是( )
| A、C2H4 |
| B、C2H2 |
| C、CH4O |
| D、C2H6O |
生产电脑芯片的材料主要是高纯硅.工业生产硅的原理为:2C+SiO2
Si+2X↑,则X的化学式是( )
| ||
| A、N2 |
| B、CO |
| C、CO2 |
| D、O2 |
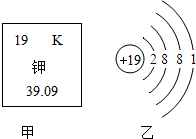 钾在自然界没有单质形态存在,钾元素以盐的形式广泛分布于陆地和海洋中,钾也是人体肌肉组织和神经组织中的重要成分之一.根据图2所示的相关信息判断,下列说法正确的是( )
钾在自然界没有单质形态存在,钾元素以盐的形式广泛分布于陆地和海洋中,钾也是人体肌肉组织和神经组织中的重要成分之一.根据图2所示的相关信息判断,下列说法正确的是( )| A、其相对原子质量为19 |
| B、图2-甲中元素符号写错,应该为K |
| C、钾原子中有19个中子 |
D、其离子结构为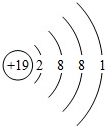 |