题目内容
 如图是水的电解实验.
如图是水的电解实验.(1)氢气与氧气的体积比是
(2)氢气与氧气的质量比是
(3)电解水是工业上制取氢气的一种方法.现有20g水(其中加了少量氢氧化钠),当液体为2g时停止通电.此时生成氢气的质量是多少?
考点:电解水实验,根据化学反应方程式的计算
专题:空气与水
分析:(1)根据电解水的实验现象来分析;(2)根据化学方程式来分析;(3)根据化学方程式进行计算来分析.
解答:解:(1)电解水时生成氧气和氢气的体积比为1:2,故填:2:1;
(2)电解水的化学方程式为:2H2O
2H2↑+O2↑,此反应中,参加反应的水、生成的氢气、氧气之间的质量比为:36:4:32=9:1:8;故填:1:8;
(3)解:参加反应的水的质量为:20g-2g=18g,
设:生成的H2的质量为x.
2H2O
2H2↑+O2↑
36 4
18g x
=
x=2g
答:生成氢气2g.
故答案为:2g.
(2)电解水的化学方程式为:2H2O
| ||
(3)解:参加反应的水的质量为:20g-2g=18g,
设:生成的H2的质量为x.
2H2O
| ||
36 4
18g x
| 36 |
| 4 |
| 18g |
| x |
x=2g
答:生成氢气2g.
故答案为:2g.
点评:本题比较全面考查了电解水的实验及实验现象和有关化学方程式的计算,通过本题的练习,加深对水的组成的认识.

练习册系列答案
相关题目
物质的化学式与相应名称均正确的一组是( )
| A、O3 氧气 |
| B、MgCl2 氯化镁 |
| C、O4Fe3 氧化铁 |
| D、NaCO3 碳酸钠 |
已知“碳13”是指原子核内含有6个质子、7个中子的碳原子,则“氦3”所指的氦原子的原子核内含有( )
| A、3个质子,3个电子 |
| B、2个质子,1个中子 |
| C、2个质子,3个中子 |
| D、3个质子,2个中子 |
地壳中含量最多的金属元素是( )
| A、铝 | B、钙 | C、氧 | D、硅 |
下列做法可以达到目的是( )
| A、用氮气作焊接金属的保护气 |
| B、加入净水剂(如明矾),使硬水转化成软水 |
| C、通常在敞口容器中验证质量守恒 |
| D、过滤时用玻璃棒搅拌,可以加快过滤速度 |
区别下列各组物质,所选择的试剂或方法错误的是( )
| 选项 | 需区别的物质 | 选择的试剂或方法 |
| A | 食醋与酒精 | 闻气味 |
| B | 空气与氧气 | 带火星的木条 |
| C | 水和双氧水 | 看颜色 |
| D | 一氧化碳与二氧化碳 | 加入少量澄清石灰水并振荡 |
| A、A | B、B | C、C | D、D |
下列关于水的说法正确的是( )
| A、水是由氢原子和氧原子构成的 |
| B、水是由两个氢元素和一个氧元素组成的 |
| C、一个水分子是由两个氢原子和一个氧原子构成的 |
| D、水分子是由氧元素和氢元素组成的 |
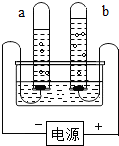 如图是“电解水实验”的装置图,根据所学知识回答问题:
如图是“电解水实验”的装置图,根据所学知识回答问题: