题目内容
8.如图是配制50克溶质质量分数为5%的氯化钠(NaCl)溶液的实验操作示意图: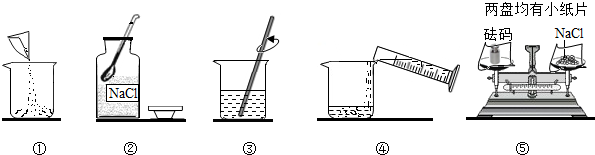
(1)请指出图中两个明显的错误处:
错误①:瓶塞正放在实验台上;错误②称量物放右盘,砝码放左盘.
(2)错误操作改正后,用上述图示的序号表示配制溶液的操作顺序②⑤①③④.
(3)需要称取氯化钠的质量是2.5 g,称量时天平出现了右盘低的现象,接下来的操作应该是④.
①左边的平衡螺丝向左调 ②右边的平衡螺丝向右调
③右盘中减少砝码 ④左盘中增加食盐
(4)下列操作会导致溶质质量分数偏低的是ABC(填字母).
A.⑤操作中所用的氯化钠含有杂质 B.①中烧杯用水洗涤后未干燥就使用
C.用量水时仰视量筒凹液面最低处读数为47.5mL D.④中向烧杯中注水时有少量水溅出.
分析 (1)为了防止瓶塞被污染,应该倒放在实验桌上;称量时,左盘应该放被称量物,右盘应该放砝码;
(2)配制溶液的操作顺序是:取出药品进行称量,量取液体倒入烧杯中,再进行溶解;
(3)根据溶质质量=溶液质量×溶质质量分数进行分析;根据托盘天平的使用进行分析;
(4)所配制的氯化钠溶液溶质质量分数大于10%,是由于所取氯化钠质量偏大、所取水的体积偏小的原因所致的结果.
解答 解:(1)图中两个操作上的错误是:瓶塞正放在实验台上;称量物放右盘,砝码放左盘.
故填:瓶塞正放在实验台上; 称量物放右盘,砝码放左盘.
(2)用上述图示的序号表示配制溶液的操作顺序是:取出氢氧化钠,进行称量,再量取水,再把氢氧化钠和水转移到烧杯中,进行溶解.
故填:②⑤①③④.
(3)配制50g 5%的氯化钠溶液时,需啊哟氯化钠的质量为50g×5%=2.5g,用托盘天平称量所需的氯化钠时,先调节天平平衡,再将砝码放在右盘,向左盘中加氯化钠,所以在称量中发现托盘天平的指针偏向右盘,说明加入的氯化钠质量少了,应该增加氯化钠,故选:④;
(4)
A.⑤操作中所用的氯化钠含有杂质,溶质的质量偏小,导致溶质质量分数偏低;
B.①中烧杯用水洗涤后未干燥就使用,由于烧杯中残留有水而使所配制溶液中水的量偏多,导致所得溶液的溶质质量分数偏低;
C.用量水时仰视量筒凹液面最低处读数为47.5mL,使所配制溶液中水的量偏大,导致所得溶液的溶质质量分数偏低;
D.④中向烧杯中注水时有少量水溅出.使所配制溶液中水的量偏小,导致所得溶液的溶质质量分数偏高.
答案:
(1)瓶塞正放在实验台上; 称量物放右盘,砝码放左盘.
(2)②⑤①③④;
(3)2.5;④;
(4)ABC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A物质的俗名 | B物质的分类 |
| 氢氧化钠的俗名--苛性钠 碳酸钠的俗名--纯碱 | HNO3--酸 NH3•H2O--碱 |
| C物质的物理性质 | D物质的鉴别 |
| 干冰能升华 氧化钙加水放热 | 化纤与纯羊毛面料燃烧 食盐与硫酸钠 加氯化钡溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 酒精挥发 玻璃破碎 | B. | 钢铁生锈 呼吸作用 | ||
| C. | 干冰升华 牛奶变酸 | D. | 光合作用 蜡烛熔化 |
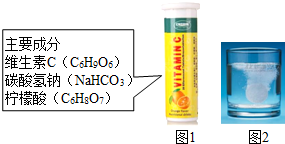 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2.
小明说:不可能含有N2,因为反应物中不含有氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有CO2.
(2)由实验②不能确定该气体中不含氧气.理由是即使气体中含有氧气,那么在二氧化碳存在时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
 海洋是丰富的化学资源宝库.通过晾晒海水,可得到含少量泥沙的粗盐.为得到比较纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作:
海洋是丰富的化学资源宝库.通过晾晒海水,可得到含少量泥沙的粗盐.为得到比较纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作: