题目内容
10. 某同学为了测定一种补钙保健食品中CaCO3的质量分数,(其包装说明如图所示)进行了如下实验:将100片该食品研碎后放入一烧杯中,向其中慢慢滴加稀盐酸,直到不再产生气泡时,共消耗稀盐酸200g,(该保健食品中其它成分不与盐酸反应)并测得烧杯内剩余物质的总质量为232.4g.请你根据以上数据计算:(Ca:40 C:12 O:16)
某同学为了测定一种补钙保健食品中CaCO3的质量分数,(其包装说明如图所示)进行了如下实验:将100片该食品研碎后放入一烧杯中,向其中慢慢滴加稀盐酸,直到不再产生气泡时,共消耗稀盐酸200g,(该保健食品中其它成分不与盐酸反应)并测得烧杯内剩余物质的总质量为232.4g.请你根据以上数据计算:(Ca:40 C:12 O:16)(1)求生成二氧化碳的质量
(2)该保健食品中CaCO3的质量分数为多少?
分析 (1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,可求得反应生成气体(CO2)的质量;
(2)根据反应的化学方程式和二氧化碳的质量可以求100片该食品中所含碳酸钙的质量,进而求出该保健食品中CaCO3的质量分数.
解答 解:(1)根据质量守恒定律反应前烧杯内物质的总质量等于烧杯内剩余物质的总质量与生成的二氧化碳的质量之和,所以反应生成气体(CO2)的质量为:100×0.5g+200g-232.4g=17.6g;
(2)设100片该保健食品中CaCO3质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 17.6g
$\frac{100}{x}$=$\frac{44}{17.6g}$
x=40g
该保健食品中CaCO3的质量分数:$\frac{40g}{100×0.5g}$×100%=80%.
故答案为:(1)17.6g;
(2)该保健食品中CaCO3的质量分数80%.
点评 本题难度不是很大,主要考查了数据地分析及根据化学方程式进行计算,培养学生的分析能力和解决问题的能力.

练习册系列答案
相关题目
8.今天又是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体,将此气体用集气瓶收集后,我们对气体展开了一系列探究:
(1)此气体是什么物质?验证它的实验方案如下
(2)我想用如图1所示仪器中的几种来制取该气体,(填序号)

则发生装置是B;收集装置是C或E.
(3)指出仪器名称:a是长颈漏斗b是集气瓶.
(4)如果用图所示的装置收集该气体,气体由A端(填“A或“B”)导入.
(5)我猜想此无色气体还可能是二氧化碳气体,可以制取它的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑若用图2装置盛满水收集氧气,气体由B端(填“A或“B”)导入.
(6)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是AC或AD.
(1)此气体是什么物质?验证它的实验方案如下
| 猜想 | 实验现象 | 实验结论及解释 |
| 此气体可能是氧气 | 把带火星的木条伸入集气瓶中,带火星的木条复燃 | 化学方程为: 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |

则发生装置是B;收集装置是C或E.
(3)指出仪器名称:a是长颈漏斗b是集气瓶.
(4)如果用图所示的装置收集该气体,气体由A端(填“A或“B”)导入.
(5)我猜想此无色气体还可能是二氧化碳气体,可以制取它的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑若用图2装置盛满水收集氧气,气体由B端(填“A或“B”)导入.
(6)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是AC或AD.
15.小红在比较金属活动性强弱的活动与探究中,先进行下表两个实验:
(1)根据上述实验可知,金属与酸反应产生气体的快慢与金属种类(或金属的活动性)、盐酸的浓度有关.
【实验三】取一烧杯,加入20mL10%的盐酸,先将打磨过的铝片放入烧杯中,观察铝片表面气泡的量,反应较长一段时间后,取出铝片,再将大小与铝片相同的且打磨过的铁片放入烧杯中,观察铁片表面气泡的量,通过比较两种金属表面产生气泡的量,来确定两者的活动性强弱.
(2)请写出铝片与盐酸反应的化学方程式2Al+6HCl=2AlCl3+3H2↑,但同学认为小红的实验三不严密,其原因是金属放入先后顺序不同,使得与其反应的盐酸浓度也可能不同.
【实验四】小红取打磨过的铝片,分别放入稀硫酸和浓硫酸中,稀硫酸中有大量气泡产生,但是浓硫酸中无明显现象,咨询老师后知道,铝片和浓硫酸发生钝化反应,生成致密的氧化铝薄膜.
(3)由此你得到什么结论:相同反应物的浓度不同,反应现象、生成物也可能不同;
(4)还有哪些因素会影响酸与金属反应是速率?请提出你的一个猜想,并设计实验方案来验证你的猜想.
猜想:温度.
实验方案:实验步骤:取大小相同的甲、乙两支试管,各加入5ml,10%的盐酸,再分别向两支试管中加入大小相同、表面积相同且均已打磨过的铝片,给其中的一个试管加热,
观察现象:两支试管中产生的气体的速率不同;
结论:温度影响酸与金属反应的速率.
| 【实验一】取相同的甲、乙试管,各加入5mL10%的盐酸,再分别向两支试管中加入大小相同且均已打磨过的铝片和锌片. | 观察到铝片表面产生的气泡比锌片表面产生的气泡多(“多”或“少”) |
| 【实验二】取相同的丙、丁试管,向试管中分别加入5mL10%及5mL5%的盐酸,再分别加入大小相同且均已打磨过的锌片. | 观察到丙试管中锌片表面产生的气泡比丁试管中多. |
【实验三】取一烧杯,加入20mL10%的盐酸,先将打磨过的铝片放入烧杯中,观察铝片表面气泡的量,反应较长一段时间后,取出铝片,再将大小与铝片相同的且打磨过的铁片放入烧杯中,观察铁片表面气泡的量,通过比较两种金属表面产生气泡的量,来确定两者的活动性强弱.
(2)请写出铝片与盐酸反应的化学方程式2Al+6HCl=2AlCl3+3H2↑,但同学认为小红的实验三不严密,其原因是金属放入先后顺序不同,使得与其反应的盐酸浓度也可能不同.
【实验四】小红取打磨过的铝片,分别放入稀硫酸和浓硫酸中,稀硫酸中有大量气泡产生,但是浓硫酸中无明显现象,咨询老师后知道,铝片和浓硫酸发生钝化反应,生成致密的氧化铝薄膜.
(3)由此你得到什么结论:相同反应物的浓度不同,反应现象、生成物也可能不同;
(4)还有哪些因素会影响酸与金属反应是速率?请提出你的一个猜想,并设计实验方案来验证你的猜想.
猜想:温度.
实验方案:实验步骤:取大小相同的甲、乙两支试管,各加入5ml,10%的盐酸,再分别向两支试管中加入大小相同、表面积相同且均已打磨过的铝片,给其中的一个试管加热,
观察现象:两支试管中产生的气体的速率不同;
结论:温度影响酸与金属反应的速率.
2.下列有关说法正确的是( )
| A. | 纯碱、火碱与稀盐酸均能发生中和反应 | |
| B. | 部分变质的氢氧化钠溶液滴入少量的稀盐酸,可能无气泡 | |
| C. | 石灰水、氢氧化钠溶液敞口放置均会因为发生化学变化而使其溶液质量增多 | |
| D. | 某无色溶液的成分可能为:KCl、K2CO3、H2SO4 |
19.森林开始发生火灾时,可以使用爆炸灭火的方法,将新型灭火弹抛到火场爆炸将火扑灭.关于爆炸灭火原因的分析不合理的是( )
| A. | 爆炸气浪降低了可燃物的着火点 | B. | 爆炸使燃烧处暂时缺氧 | ||
| C. | 炸起的沙土覆盖可燃物,隔绝空气 | D. | 爆炸气浪降低了可燃物的温度 |
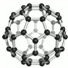 C60的模型如图所示,每个碳原子和相邻的3个碳原子以小棍结合.若要搭建一个这样的模型,需要代表碳原子的小球60个,需要代表化学键的连接小球的小棍90根.
C60的模型如图所示,每个碳原子和相邻的3个碳原子以小棍结合.若要搭建一个这样的模型,需要代表碳原子的小球60个,需要代表化学键的连接小球的小棍90根.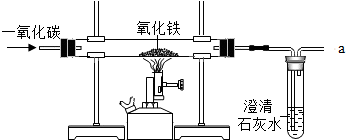

 所表示的粒子符号为Al,位于周期表中第三周期.
所表示的粒子符号为Al,位于周期表中第三周期.