题目内容
8.丙酸钠(C3H5O2Na)是一种常见的食品添加剂,根据化学式回答:(1)丙酸钠中碳、氢、氧三种元素的质量比为36:5:32;
(2)丙酸钠的相对分子质量为96.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
解答 解:(1)丙酸钠中碳、氢、氧元素的质量比为(12×3):(1×5):(16×2)=36:5:32.
(2)丙酸钠的相对分子质量为12×3+1×5+16×2+23=96.
故答案为:(1)36:5:32;(2)96.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.从2012年1月1日起,欧盟将正式征收航空业碳排放税,几乎所有起飞或降落在欧盟境 内的国际空运活动都需要纳入欧洲碳排放交易体系.航空“碳排放税”顾名思义就是指航空燃油燃烧排放二氧化碳征收的税,它是通过对航空燃油碳含量的比例来征税,从而减少燃料消耗和二氧化碳排放.下列有关说法正确的是( )
| A. | 二氧化碳是一种温室气体 | |
| B. | 减少二氧化碳排放最好是禁止使用石油等燃料 | |
| C. | 固体二氧化碳称为冰 | |
| D. | 大量排放二氧化碳是引起大气污染的主要因素 |
16.现有X,Y,Z三种金属,将X,Y分别放入稀盐酸中,X表面无明显变化,Y表面有气泡产生,将X,Y放入Z的硝酸盐溶液中,X,Y表面均无明显变化,这三种金属的活动性由强到弱的顺序为( )
| A. | XYZ | B. | ZYX | C. | YXZ | D. | ZXY |
13.下列过程中有一个变化与其它变化不同的是( )
| A. | 光合作用 | B. | 浓硫酸做干燥剂 | ||
| C. | 用食醋除水垢 | D. | 用灼烧法鉴别羊毛和合成纤维 |
20.下列有关元素的说法正确的是( )
| A. | 不同元素间的本质区别是粒子的核外电子数不同 | |
| B. | 元素的化学性质主要取决于原子的核外电子数 | |
| C. | 空气、海水、地壳中含量最多的元素都是氧元素 | |
| D. | 硒(Se)属于人体的必需微量元素,应合理摄入 |
18.下列有关实验设计和操作的叙述中,正确的是( )
| A. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| B. | 将Fe(OH)3加入到滴有酚酞试液的蒸馏水中,溶液显红色 | |
| C. | 实验室做氢气还原氧化铁的实验时,应先通入氢气,过一会儿再给氧化铁加热 | |
| D. | 配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 |
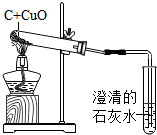 某中学化学兴趣小组按照课本实验方法,做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.
某中学化学兴趣小组按照课本实验方法,做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现.他们决定对这个实验进行探究和改进.