题目内容
18.近几年,我国酸雨污染较为严重.有关资料显示,我国的酸雨主要是因为大量燃烧含硫量高的煤而形成的.【提出问题】通过实验证明煤中含有碳元素和硫元素.
【查阅资料】①“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色)该反应的化学方程式为:
5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2
 ”.资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:H2SO4.(在上教版九年级化学教材中即用此原理检验含硫火柴中的硫元素.)二氧化硫还能使澄清石灰水变浑浊.
”.资料上这个化学方程式中最后一种物质的化学式印刷不清楚,请推测其化学式:H2SO4.(在上教版九年级化学教材中即用此原理检验含硫火柴中的硫元素.)二氧化硫还能使澄清石灰水变浑浊.②用化学方程式表示出二氧化硫形成硫酸型酸雨的过程(任写一种):SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4.
根据上述资料,甲同学和乙同学分别设计实验方案进行探究.
(1)甲同学:
【进行实验】甲同学进行了如图1所示A、B两步实验:
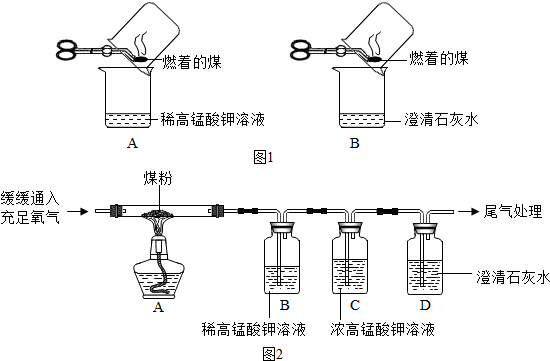
【观察现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊.
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.
你认为该实验方案是否合理并简述理由:不合理.因为二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素.
(2)乙同学:
【进行实验】乙同学进行了如图2所示实验(部分装置在图中略去):B装置的作用是检验二氧化硫,C装置的作用是除去二氧化硫并检验二氧化硫是否除尽.
【观察现象】
(请写出B、C、D中的现象)B中溶液褪色,C中溶液仍为紫红色(或颜色变浅),D中溶液变浑浊.
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.
分析 本题以实验探究的形式,检验煤的碳元素和硫元素,需要我们知道质量守恒定律;会书写化学反应式;了解试验装置的合理性;会分析各种试验现象.
解答 解:[查阅资料]①据物质的质量守恒定律可知,其化学式为:H2SO4②二氧化硫能使澄清石灰水变浑浊,一定生成了沉淀物CaSO3.故化学反应式为:SO2+Ca(OH)2═CaSO3↓+H2O
(1)据资料知,A试验中的稀高锰酸钾溶液褪色,说明煤中含硫元素.B试验中的澄清石灰水变浑浊,说明煤中可能含有碳元素也可能含有硫元素.故不合理.
故答案为:因为二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素.
(2)二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),故B装置的作用是:检验二氧化硫;浓高锰酸钾溶液可与二氧化硫反应除去二氧化硫,高锰酸钾溶液又可检验二氧化硫的存在.故C装置的作用是:除去二氧化硫并检验二氧化硫是否除尽;
观察现象:加热碳粉生成二氧化硫,二氧化硫与稀高锰酸钾溶液反应并使其褪色.二氧化硫在B中已与高锰酸钾溶液反应,C中的浓高锰酸钾溶液仍为紫红色.煤粉燃烧生成的二氧化碳可使澄清石灰水变浑浊.
故B、C、D中的现象分别为:B中溶液褪色,C中溶液仍为紫红色(或颜色变浅),D中溶液变浑浊;
答案:
①H2SO4;②SO2+H2O═H2SO3;2H2SO3+O2═2H2SO4;
(1)不合理.因为二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素.
(2)检验二氧化硫; 除去二氧化硫并检验二氧化硫是否除尽;
B中溶液褪色,C中溶液仍为紫红色(或颜色变浅),D中溶液变浑浊.
点评 本题以实验探究的形式,检验物质的存在和物质的性质.培养了学生的动手能力和动脑思考的能力.

练习册系列答案
相关题目
9.下列观点你不赞成的是( )
| A. | 化学变化的实质是原子的重新组合的过程 | |
| B. | 在与外界隔绝的条件下,物质间不论发生何种反应,其总质量保持不变 | |
| C. | 在化学反应后,生成的各物质的质量总和,一定等于反应物的质量 | |
| D. | 化学变化前后,元素的种类不会改变 |
6.化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,如${\;}_{6}^{13}C$表示核内有6个质子和7个中子的碳原子.下列关于${\;}_{53}^{131}$I和${\;}_{53}^{127}$I的说法中错误的是( )
| A. | 中子数相同 | B. | 属于同种元素 | C. | 核外电子数相同 | D. | 质子数相同 |
13.区别一瓶蒸馏水和一瓶矿泉水,不能使用的方法是( )
| A. | 蒸发 | B. | 加肥皂水 | C. | 尝味道 | D. | 测导电性 |