题目内容
2.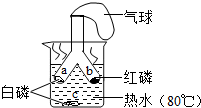 如图所示为探究燃烧条件的实验方案.将白磷和红磷分装于Y形管的两支管中,管口牢系小气球,将两支管同时深入热水中.
如图所示为探究燃烧条件的实验方案.将白磷和红磷分装于Y形管的两支管中,管口牢系小气球,将两支管同时深入热水中.(1)a(选填“a”、“b”、或“c”)处有燃烧现象出现,该燃烧反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)小气球的作用是:①平衡Y形管内外的压强;②防止污染空气.
(3)对比a处与b处(选填“a”、“b”、或“c”)的现象,说明可燃物燃烧需要达到着火点.
(4)实验后,将烧杯中的热水倒出后,c处的白磷开始燃烧,c处白磷燃烧的原因是达到着火点的白磷接触空气就剧烈燃烧起来.
分析 (1)根据燃烧的条件分析;根据磷燃烧生成的五氧化二磷会污染空气;根据燃烧的条件分析,可燃物与氧气接触且温度达到着火点;
解答 解:(1)a处的白磷温度达到了着火点,能与氧气接触,所以能燃烧,由于试管内的氧气的量少,该处燃着的磷会很快熄灭;磷燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)由于磷燃烧生成的五氧化二磷会污染空气,所以管口的小气球可以防止P2O5进入空气,从而使该实验绿色化,故填:防止污染空气.
(3)说明可燃物燃烧需要达到着火点,只要对比ab两处,白磷燃烧,红磷不燃烧,其他条件都相同,只有可燃物不同,从而证明可燃物燃烧需要达到着火点,故填:a;b;
(4)在水下的白磷温度达到了着火点不燃烧的原因是没有与氧气接触,白磷刚露出水面就剧烈燃烧起来原因是有了氧气,温度已经达到了着火点,所以白磷刚露出水面就剧烈燃烧起来,故填:达到着火点的白磷接触空气就剧烈燃烧起来.
点评 题考查了物质燃烧的条件,物质燃烧的三个条件缺一不可.

练习册系列答案
相关题目
6.某化学反应可表示为:二氧化碳+水→M+氧气,根据以上信息,下列关于M组成的说法中正确的是( )
| A. | 一定含有C、H元素,可能含有O元素 | B. | 只含有C、H元素 | ||
| C. | 含有C、H、O三种元素 | D. | 无法确定 |
7.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )
| A. | NaCl溶液(MgCl2)-加入过量的NaOH溶液,过滤,滤液中加稀盐酸至中性 | |
| B. | 氧气(水蒸气)-通过装有足量无水氯化钙的干燥管 | |
| C. | CaO固体(CaCO3)-高温充分煅烧 | |
| D. | 氢气(氯化氢气体)-依次通过足量的NaHCO3溶液和浓硫酸 |
7.化学实验小组同学为了验证“盐酸除去铁块表面锈迹后黄色溶液的成分”,进行了如下探究.
【查阅资料】
①Fe+2FeCl3═3FeCl2.
②在酸性条件下,FeCl2可以使高锰酸钾溶液褪色,并生成FeCl3.
③FeCl3溶液可以与KSCN溶液反应,溶液变为血红色.
【猜想与假设】黄色液体中含有FeCl3、FeCl2和HCl.
【进行实验】
(1)写出氧化铁与盐酸反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(2)丙同学试管②中的实验现象为产生大量气泡.
(3)三位同学的方案不合理的是甲和乙,原因是甲:依据资料②,FeCl2和高锰酸钾反应时生成了FeCl3,无法证明黄色溶液中有FeCl3
乙:依据资料①,加入Fe粉时,Fe与盐酸或FeCl3反应生成了FeCl2,无法证明黄色溶液中有FeCl2.
【实验反思】
(4)在混合物中,各种成分能(填“能”或“不能”)保持各自的化学性质.
(5)在混合体系中检验多种物质存在时,要考虑物质间的相互影响;物质检验的顺序;所加检验试剂的用量等(答出1条即可).
【查阅资料】
①Fe+2FeCl3═3FeCl2.
②在酸性条件下,FeCl2可以使高锰酸钾溶液褪色,并生成FeCl3.
③FeCl3溶液可以与KSCN溶液反应,溶液变为血红色.
【猜想与假设】黄色液体中含有FeCl3、FeCl2和HCl.
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 | |
| 甲同学 | 取1支试管,加入少量黄色液体,然后滴加高锰酸钾溶液,再滴加KSCN溶液 | 高锰酸钾溶液褪色,溶液变为血红色 | 黄色溶液中有HCl、FeCl2和FeCl3 |
| 乙同学 | 取2支试管,分别加入少量黄色溶液.再向试管①中滴加KSCN溶液;向试管②中加入铁粉,再滴加高锰酸钾溶液 | 试管①中溶液变为血红色;试管②中产生大量气泡,高锰酸钾溶液褪色 | 黄色溶液中有HCl、FeCl2和FeCl3 |
| 丙同学 | 取3支试管,分别加入少量黄色溶液.再向试管①中滴加KSCN溶液;试管②中加入铁粉;试管③中滴加高锰酸钾溶液 | 试管①中溶液变为血红色;试管②…;试管③中高锰酸钾溶液褪色 | 黄色溶液中有HCl、FeCl2和FeCl3 |
(2)丙同学试管②中的实验现象为产生大量气泡.
(3)三位同学的方案不合理的是甲和乙,原因是甲:依据资料②,FeCl2和高锰酸钾反应时生成了FeCl3,无法证明黄色溶液中有FeCl3
乙:依据资料①,加入Fe粉时,Fe与盐酸或FeCl3反应生成了FeCl2,无法证明黄色溶液中有FeCl2.
【实验反思】
(4)在混合物中,各种成分能(填“能”或“不能”)保持各自的化学性质.
(5)在混合体系中检验多种物质存在时,要考虑物质间的相互影响;物质检验的顺序;所加检验试剂的用量等(答出1条即可).
14.同学们在学习Ca(OH)2的化学性质时,对Ca(OH)2溶液和Na2 CO3溶液反应后溶液中溶质的成分进行探究.请你一同探究并回答下列问题:
【提出问题】滤液中的溶质是什么物质?
【查阅资料】①Ca(NO3)2溶液呈中性. ②Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3
【猜想假设】甲同学认为只含有NaOH;乙同学认为只含有NaOH,Ca(OH)2;丙同学认为含有NaOH、Ca(OH)2、Na2CO3;你认为可能含有NaOH和Na2CO3
【分析讨论】丁同学认为丙同学的猜想肯定是不合理的,理由是如果氢氧化钙和碳酸钠同时存在时会发生化学反应.
【实验设计】请你设计一个简单的实验来验证你的猜想是正确的.
甲同学也针对自己的猜想进行了如下实验.
你认为甲同学的实验结论是否正确?不正确(填“正确”或“不正确”),理由是如果含有NaOH和Ca(OH)2时或含有NaOH和Na2CO3时,滴加少量的稀盐酸时也是无明显现象.
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑反应物是否有剩余.
【提出问题】滤液中的溶质是什么物质?
【查阅资料】①Ca(NO3)2溶液呈中性. ②Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3
【猜想假设】甲同学认为只含有NaOH;乙同学认为只含有NaOH,Ca(OH)2;丙同学认为含有NaOH、Ca(OH)2、Na2CO3;你认为可能含有NaOH和Na2CO3
【分析讨论】丁同学认为丙同学的猜想肯定是不合理的,理由是如果氢氧化钙和碳酸钠同时存在时会发生化学反应.
【实验设计】请你设计一个简单的实验来验证你的猜想是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中, 滴加足量的硝酸钙溶液,再滴入几滴酚酞试液 | 出现白色沉淀,酚酞试液变红色 | 猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,滴加少量的稀盐酸 | 无明显现象 | 猜想正确 |
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外,还需要考虑反应物是否有剩余.