题目内容
2.在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验补充完整.【实验目的】铁生锈条件的探究.
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象
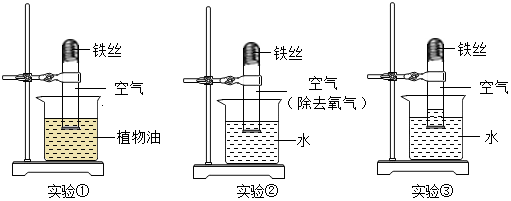
【实验现象】实验①②无明显现象,实验③中铁丝生锈,且试管内空气体积减小.
【实验结论】铁生锈实际上是铁与空气中的水和氧气(填名称)发生反应的结果.
【实验思考】
(1)当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的$\frac{1}{5}$.
(2)该实验创新之处在于:可根据铁丝表面的铁锈和试管内液面上升两种现象来判断铁丝反应进行的情况.
(3)铝比铁活泼,但铝难腐蚀,原因是铝易被氧气氧化生成致密的氧化铝保护膜.
(4)某炼铁厂每天生产含杂质4%的生铁400t,?每天需要含氧化铁70%的赤铁矿多少吨??如果改用含有杂质为25%的磁铁矿则需要多少吨这样的磁铁矿?
分析 根据铁生锈的条件进行分析.铁在有水和氧气并存时易生锈,空气中氧气的体积分数大约占$\frac{1}{5}$,铁生锈消耗氧气,导致试管内的压强减小,液面会上升,进入试管的水的体积大约占试管体积的$\frac{1}{5}$;根据铝的性质以及铁元素守恒进行分析解答即可.
解答 解:【实验结论】铁生锈是铁与水和氧气共同反应的结果,故填:水和氧气;
【实验思考】(1)铁生锈消耗氧气,导致试管内的压强减小,液面会上升,故当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的五分之一,故填:$\frac{1}{5}$;
(2)该实验可以根据铁生锈以及试管内液面上升来判断铁丝反应进行的情况,故填:试管内液面上升;
(3)铝易被氧气氧化生成致密的氧化铝保护膜,故难以腐蚀,故填:铝易被氧气氧化生成致密的氧化铝保护膜;
(4)设需要含氧化铁70%的赤铁矿的质量为x
x×70%×$\frac{56×2}{56×2+16×3}$=400t×(1-4%) x=783.7t;
设需要含有杂质为25%的磁铁矿的质量为y
y×$(1-25%)×\frac{56×3}{56×3+16×4}$=400t×(1-4%) y=707t
答:需要含氧化铁70%的赤铁矿的质量为783.7t;需要含有杂质为25%的磁铁矿的质量为707t.
点评 本题考查的是金属的锈蚀因素以及根据化学式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
5.小红同学用托盘天平称量食盐时,错误的将食盐放在右盘里,砝码放在左盘里,称得食盐质量为10.6g(1g以下用游码),食盐的实际质量应为( )
| A. | 10.6g | B. | 10g | C. | 9.4g | D. | 11.2g |
3.今年冬天,雾霾天气肆虐全国许多地方,环境保护是人类共同的责任,下列环境措施中,你认为不可行的是( )
| A. | 大力实施绿化工程防治扬尘污染 | B. | 分类回收垃圾并进行露天焚烧 | ||
| C. | 多使用清洁能源代替煤和石油 | D. | 使用燃煤脱硫技术防治SO2污染 |
7. 铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件.
铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件.
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关.
【进行实验】通过控制与铜片接触的物质,利用如图装置(铜片长8cm,宽lcm,试管容积为20mL),分别进行下列7个实验,并持续观察30天.
【解释与结论】
(1)实验3中,要使用经煮沸并迅速泠却的蒸馏水,原因是除去水中的氧气.
(2)实验5的目的是探究铜生锈是否是铜与水和二氧化碳共同反应的结果.
(3)通过上述实验,得出铜生绣的条件是与水、氧气和二氧化碳共同反应.
【反思与评价】
(4)请写出一种防止铜制品锈蚀的方法涂油.
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3.由此,你认为上述实验中只需进行实验5、7(填实验编号),就可探究出铜生锈条件,理甶是碱式碳酸铜的化学式中含有碳、氢元素,由元素守恒可以知道,铜生锈的过程中一定有二氧化碳和水参加反应,故只需要进行实验5和7即可知道铜生锈条件是否需要氧气的参加.
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因可能是空气中氧气、二氧化碳和水蒸气的含量较低.
 铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件.
铜片在潮湿的空气中久置,表面会产生绿色的铜锈.某小组同学设计并进行实验,探究铜生锈的条件. 【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关.
【进行实验】通过控制与铜片接触的物质,利用如图装置(铜片长8cm,宽lcm,试管容积为20mL),分别进行下列7个实验,并持续观察30天.
| 编号 | 主要实验操作 | 实验现象 |
| 1 | 充满纯净的O2 | 铜片均无明显变化 |
| 2 | 充满纯净的CO2 | |
| 3 | 充满经煮沸并迅速冷却的蒸馏水 | |
| 4 | 加入蒸馏水5mL (液面未浸没铜片),再充满O2 | |
| 5 | 加入经煮沸并迅速泠却的蒸馏水5ml,再充满CO2 | |
| 6 | 充入10mLO2,再充入10mLCO2 | |
| 7 | 加入蒸馏水5mL,再依次充入l0mLCO2和10mLO2 | 铜片生锈,且水面附近锈蚀最严重 |
(1)实验3中,要使用经煮沸并迅速泠却的蒸馏水,原因是除去水中的氧气.
(2)实验5的目的是探究铜生锈是否是铜与水和二氧化碳共同反应的结果.
(3)通过上述实验,得出铜生绣的条件是与水、氧气和二氧化碳共同反应.
【反思与评价】
(4)请写出一种防止铜制品锈蚀的方法涂油.
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3.由此,你认为上述实验中只需进行实验5、7(填实验编号),就可探究出铜生锈条件,理甶是碱式碳酸铜的化学式中含有碳、氢元素,由元素守恒可以知道,铜生锈的过程中一定有二氧化碳和水参加反应,故只需要进行实验5和7即可知道铜生锈条件是否需要氧气的参加.
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因可能是空气中氧气、二氧化碳和水蒸气的含量较低.
12.下列关于氧气物理性质的叙述,正确的是( )
| A. | 液态氧是没有颜色的 | |
| B. | .在通常状况下氧气是没有颜色,没有气味的气体 | |
| C. | .氧气的密度略小于空气 | |
| D. | .氧气极易溶于水 |
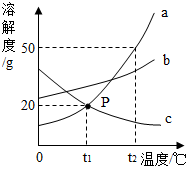 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: 如图是活性炭净水器示意图,其中活性炭的作用是:吸附色素和异味、滤去不溶性杂质.用此装置得到了澄清透明的水,该水是否为纯水,理由是不是纯水,净化后的水中含有可燃性的杂质.
如图是活性炭净水器示意图,其中活性炭的作用是:吸附色素和异味、滤去不溶性杂质.用此装置得到了澄清透明的水,该水是否为纯水,理由是不是纯水,净化后的水中含有可燃性的杂质.