题目内容
为粗略测量空气中O2与N2的体积比,某学生设计了如 图 所示的实验装置进行实验.实验时,先关闭弹簧夹,将螺旋状的铜 丝在酒精灯上灼烧后迅速插入大试管,接触试管底部的过量的白磷(白磷在空气中燃烧的温度为40℃),然后立即塞紧橡皮塞,可观察到大试管中产生大量的白烟.试回答以下问题:(1)写出上述反应化学方程式:______ 2P2O5

【答案】分析:(1)结合实际反应书写方程式.
(2)由于燃烧消耗氧气使瓶内气压减小.
(3)防止试管炸裂.
(5)太少氧气会不能完全消耗,导致进入的水较少,装置漏气同样也会使水进入的偏小,白磷太多时由于产生的热量太多也会导致塞子被冲出.
解答:解:(1)白磷燃烧后产物是五氧化二磷.
故答案为:4P+5O2 2P2O5
2P2O5
(2)由于氧气被耗尽,且氧气中空气体积的五分之一,所以水会进入试管的,剩余的气体主要是氮气,约占空气体积的五分之四.
故答案为:水进入试管中约五分之一;1:4
(3)由于燃烧时会产生大量的热,容易炸裂试管,所以要放入少量的细沙.
故答案为:隔热,防止白磷燃烧放出大量热导致试管炸裂.
(4)白磷量少时会导致氧气消耗不完全,测量的数据不到五分之一,白磷量多时则会出现热量放出太多,容易把试管上的塞子冲出.
故答案为:偏小;装置漏气放热太多而把塞子冲出.
点评:此题是空气成分检验考查题,解题的关键是对整个实验的原理操作及注意事项的掌握,属基础性实验知识考查题.
(2)由于燃烧消耗氧气使瓶内气压减小.
(3)防止试管炸裂.
(5)太少氧气会不能完全消耗,导致进入的水较少,装置漏气同样也会使水进入的偏小,白磷太多时由于产生的热量太多也会导致塞子被冲出.
解答:解:(1)白磷燃烧后产物是五氧化二磷.
故答案为:4P+5O2
 2P2O5
2P2O5(2)由于氧气被耗尽,且氧气中空气体积的五分之一,所以水会进入试管的,剩余的气体主要是氮气,约占空气体积的五分之四.
故答案为:水进入试管中约五分之一;1:4
(3)由于燃烧时会产生大量的热,容易炸裂试管,所以要放入少量的细沙.
故答案为:隔热,防止白磷燃烧放出大量热导致试管炸裂.
(4)白磷量少时会导致氧气消耗不完全,测量的数据不到五分之一,白磷量多时则会出现热量放出太多,容易把试管上的塞子冲出.
故答案为:偏小;装置漏气放热太多而把塞子冲出.
点评:此题是空气成分检验考查题,解题的关键是对整个实验的原理操作及注意事项的掌握,属基础性实验知识考查题.

练习册系列答案
 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
 为粗略测量空气中O2与N2的体积比,某学生设计了如 图 所示的实验装置进行实验.实验时,先关闭弹簧夹,将螺旋状的铜 丝在酒精灯上灼烧后迅速插入大试管,接触试管底部的过量的白磷(白磷在空气中燃烧的温度为40℃),然后立即塞紧橡皮塞,可观察到大试管中产生大量的白烟.试回答以下问题:
为粗略测量空气中O2与N2的体积比,某学生设计了如 图 所示的实验装置进行实验.实验时,先关闭弹簧夹,将螺旋状的铜 丝在酒精灯上灼烧后迅速插入大试管,接触试管底部的过量的白磷(白磷在空气中燃烧的温度为40℃),然后立即塞紧橡皮塞,可观察到大试管中产生大量的白烟.试回答以下问题: 为粗略测量空气中O2与N2的体积比,某学生设计了如右图所示的实验装置进行实验.实验时,先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.试回答以下问题:
为粗略测量空气中O2与N2的体积比,某学生设计了如右图所示的实验装置进行实验.实验时,先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.试回答以下问题: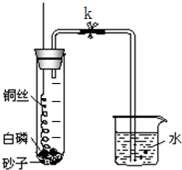 为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.
为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟. 为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.
为粗略测量空气中O2与N2的体积比,某学生设计了如图所示的实验装置进行实验.实验时,先关闭弹簧夹k,将螺旋状的铜丝在酒精灯火焰上灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞.由于白磷的着火点(燃烧所需的最低温度)比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟.