题目内容
1.如图是配制 50 克溶质质量分数为 8%的氯化钠(NaCl)溶液的有关操作示意图: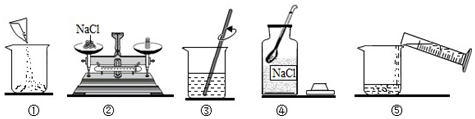
(1)需要称取氯化钠的质量是4g,称量时出现了右盘低的现象,接下来的操作应 该是:继续向左盘中增加氯化钠,使天平平衡.
(2)配制氯化钠溶液的正确顺序是④②①⑤③(用上述图示的序号表示).
(3)经检测,所配制的溶液溶质质量分数偏小,其原因可能有BC.
A.称量时使用了生锈的砝码B.称量时,砝码端忘垫质量相同的纸片 C.量取水时,仰视读数D.装瓶时,有少量溶液洒出.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量,结合托盘天平的使用方法,进行分析解答.
(2)根据配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
(3)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制50 克溶质质量分数为8%的氯化钠溶液,需氯化钠的质量=50g×8%=4g.
称量时出现了右盘低的现象,说明氯化钠的质量小于砝码的质量,接下来的操作应该是继续向左盘中增加氯化钠,使天平平衡.
(2)配制50克溶质质量分数为8%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故正确顺序是④②①⑤③.
(3)A.称量时使用了生锈的砝码,会造成氯化钠的质量增加,会导致所得溶液溶质质量分数偏大.
B.称量时,砝码端没垫相同的纸片,氯化钠和纸片的质量等于砝码和游码的质量,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小.
C.量取水时,仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
D.溶液具有均一性,装瓶时有少量溶液洒出,溶质质量分数不变.
故答案为:(1)4;继续向左盘中增加氯化钠,使天平平衡;(2)④②①⑤③;(3)BC.
点评 本题难度不大,明确一定溶质质量分数溶液的配制的步骤(计算、称量、溶解)、注意事项等是正确解答此类题的关键.

练习册系列答案
相关题目
11.为了探究影响固体溶解性的因素,某同学实际了如下三组实验
(1)分析上表,第一组实验研究的因素是溶剂种类;
(2)有上述实验可知,影响固体溶解性的因素是①②④;
①温度②加入溶剂种类③加入溶剂质量④假如固体种类⑤加入固体质量
(3)在第二组试验中,该同学按照如下步骤进行实验(假设溶液损失不计)
①用电子天平称取10.0g的硝酸钾,放入烧杯中;
②量取10.0ml水,倒入上述烧杯中,称量烧杯、硝酸钾和谁的总质量为m1g;
③胶版纸硝酸钾不在溶解为止;
④过滤,称量所得硝酸钾溶液和少北的总质量为m2g;
⑤计算:m1-m2=6.9g(结合第二组实验数据进行分析).
将溶质改为食盐,重复上述步骤进行试验.由实验可知,20℃是食盐的溶解性>(填“>”、“=”或“<”)硝酸钾的溶解性.
(4)根据上述实验,以下推论正确的是AD.
A.20℃时,氯化钠的溶解度为36g
B.20℃时,硝酸钾饱和溶液的溶质质量分数为31%
C.第三组实验中的硝酸钾溶液为80℃时的饱和溶液
D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等.
| 因素 | 第一组 | 第二组 | 第三组 | ||
| 实验温度 | 20℃ | 20℃ | 20℃ | 20℃ | 80°C |
| 加入溶剂种类 | 水 | 酒精 | 水 | 水 | 水 |
| 加入溶剂质量 | 20g | 20g | 10g | 10g | 10g |
| 加入固体种类 | 硝酸钾 | 硝酸钾 | 硝酸钾 | 食盐 | 硝酸钾 |
| 加入固体质量 | 10g | 10g | 10g | 10g | 10g |
| 溶解固体质量 | 6.2g | 0g | 3.1g/ | 3.6g | 10g |
(2)有上述实验可知,影响固体溶解性的因素是①②④;
①温度②加入溶剂种类③加入溶剂质量④假如固体种类⑤加入固体质量
(3)在第二组试验中,该同学按照如下步骤进行实验(假设溶液损失不计)
①用电子天平称取10.0g的硝酸钾,放入烧杯中;
②量取10.0ml水,倒入上述烧杯中,称量烧杯、硝酸钾和谁的总质量为m1g;
③胶版纸硝酸钾不在溶解为止;
④过滤,称量所得硝酸钾溶液和少北的总质量为m2g;
⑤计算:m1-m2=6.9g(结合第二组实验数据进行分析).
将溶质改为食盐,重复上述步骤进行试验.由实验可知,20℃是食盐的溶解性>(填“>”、“=”或“<”)硝酸钾的溶解性.
(4)根据上述实验,以下推论正确的是AD.
A.20℃时,氯化钠的溶解度为36g
B.20℃时,硝酸钾饱和溶液的溶质质量分数为31%
C.第三组实验中的硝酸钾溶液为80℃时的饱和溶液
D.20℃的任意一杯饱和硝酸钾溶液中,溶质与溶剂的质量比一定相等.
12.下列实验现象的描述正确的是( )
| A. | 碳在氧气中燃烧发出白光,产生白烟 | |
| B. | 铁丝在氧气中燃烧火星四射,生成黑色固体 | |
| C. | 将铁丝伸入稀盐酸中,溶液变成黄色 | |
| D. | 铝丝伸入硫酸铜溶液中,铝的表面有铜析出 |
9.兴趣活动小组设计并完成了如下实验(装置气密性良好,药品足量):
| 操作 | 现象 | 结论 | 装置 |
| 实验一: 同时将Ⅰ中5mL5%的过氧化氢溶液和Ⅱ中5mL15%的过氧化氢溶液注入各盛有0.5g二氧化锰的甲、乙中,关闭弹簧夹. | 发现烧杯中右侧导管口产生气泡的速率比左侧快. | 化学反应速率与 反应物浓度有关; 该反应的化学方程式为 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. | 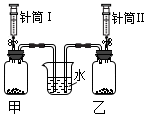 |
| 操作 | 现象 | 现象分析 | 装置 |
| 实验二: 先将稀盐酸注入甲,关闭弹簧夹;再将水注入乙,关闭弹簧夹. 注意:注入液体后,甲、乙导管口均处于液面以下. | 甲中液体先流入烧杯,乙中液体后流入烧杯,然后观察到烧杯中先无明显现象,后有白色沉淀产生. | 乙中液体流入烧杯的原因是 氢氧化钠溶于水,放出热量,使得瓶内压强大于外界压强; 甲中流入烧杯的液体溶质的化学式是 MgCl2HCl. | 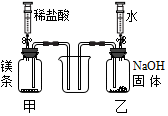 |
16.2016 年 10 月 17 日,青海玉树藏族自治州杂多县发生 6.3 级地震.当地生产生活受到很 大影响,尤其是饮用水的污染和短缺.下列几个步骤将河水转化为饮用水:①化学沉降
(用明矾)②消毒杀菌(用漂白粉)③自然沉降④加热煮沸.以上处理过程最合理的顺 序是( )
(用明矾)②消毒杀菌(用漂白粉)③自然沉降④加热煮沸.以上处理过程最合理的顺 序是( )
| A. | ③②①④ | B. | ③①②④ | C. | ③①④② | D. | ①③②④ |
6.氯化钠的下列用途中,主要反映其具有杀菌防腐作用的是( )
| A. | 制生理盐水 | B. | 作调味剂 | C. | 腌制鱼肉 | D. | 制取氢氧化钠 |
13.小明同学在做氢氧化钾溶液和稀盐酸反应的实验时,为了确认反应后得到的溶液中是否含盐酸,取少量反应后的溶液于试管中,用某种试剂进行检验.下表是小明同学设计的实验方案,其中错误的是( )
| 实验方案 | 使用的试剂 | 判断的方法 |
| A | CuO | 若CuO溶解,溶液变成蓝色,表明盐酸已过量 |
| B | pH试纸 | 若pH<7,表明盐酸已经过量 |
| C | 紫色石蕊试剂 | 若溶液变成红色,表明盐酸已经过量 |
| D | AgNO3溶液 | 若产生白色沉淀,表明盐酸已经过量 |
| A. | A | B. | B | C. | C | D. | D |
10.如图实验操作错误的是( )
| A. |  滴加液体 | B. |  检查气密性 | C. |  加热液体 | D. |  量取9.5ml液体 |
11.为了预防樱桃在成熟期发生果实开裂,果农常施钾肥,下列属于钾肥的是( )
| A. | NH4NO3 | B. | CO(NH2)2 | C. | KNO3 | D. | K2CO3 |