题目内容
11.下列五种说法:①FeO、Fe3O4、Fe2O3三种物质中的FeO中的铁元素质量分数最大;②电解水实验中与电源负极相连的一端产生的气体能燃烧;③过滤操作中用到了三种玻璃仪器;④原子既可以通过构成分子再构成物质,也可以直接构成物质.⑤地壳中含量最多的金属元素为铝.其中正确的有( )| A. | 两个 | B. | 三个 | C. | 四个 | D. | 五个 |
分析 ①根据铁的化合物的化学式,通过变形使铁的原子个数相等,然后比较化合物中其它元素的原子的相对原子质量之和,其它原子的相对原子质量之和越大的,在该化合物中铁元素的质量分数就越小.
②根据电解水实验的现象和结论,来判断本题的正误.正极产生氧气,负极产生氢气,氢气和氧气的体积比为2:1;
③根据过滤操作的原理、使用的仪器进行分析解答即可;
④考虑分子由原子构成,原子也可直接构成物质;
⑤根据地壳中各元素含量的排序及元素的分类判断.
解答 解:
①在FeO、Fe2O3、Fe3O4三种物质中,将化学式变形得Fe6O6、Fe6O9、Fe6O8,因32×6>16×9>16×8>,所以含铁的质量分数最大的是:FeO,说法正确;
②在电解水时,与电源正极相连的一端产生的气体较少是氧气,与电源负极相连的一端产生的气体较多是氢气,能燃烧,说法正确;
③过滤中用到的仪器有:铁架台、玻璃棒、烧杯、漏斗等,其中用到的三种玻璃仪器是漏斗、烧杯、玻璃棒,说法正确;
④原子既可以通过构成分子再构成物质,也可以直接构成物质,说法正确;
⑤地壳含量较多的元素按含量从高到低的排序为:氧、硅、铝、铁、钙,在金属元素中含量最多的是铝,说法正确.
故选D.
点评 本题难度不大,考查化学式的有关计算,将化学式进行变形,使铁原子个数化为相等是正确快速解答的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.某反应的微观示意图如图,有关说法不合理的是( )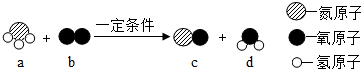

| A. | 生成物都是氧化物 | |
| B. | 该化学反应前后元素种类、原子种类都没有变化 | |
| C. | 化学反应前后分子数目相等 | |
| D. | 反应物是NH3和O2 |
6.小明利用网络,了解到铜器外置后表面会出现一层绿色物质,这层绿色物质俗称铜绿.小明邀请你一起探究铜绿的性质.
【提出问题】铜绿具有什么性质?
【猜想与假设】根据网络资料,小明猜想铜绿具有如下性质:
(1)铜绿难溶于水;(2)铜绿受热分解;(3)铜绿能与稀盐酸反应.
【实验用品】铜绿、稀盐酸、澄清石灰水、药匙、试管、酒精灯、铁架台、烧杯、玻璃片、带导管的单孔塞、胶头滴管、试管刷、火柴.
【实验与记录】
【分析与讨论】
(1)本次探究中,涉及取用药品.粉末状固体取用的操作,将试管竖直放置,用药匙将铜绿从试管口倒入试管中,可能带来的后果是药品附着在试管壁上.
(2)酒精灯时化学实验常见的热源,加热时应该利用酒精灯的外焰加热,熄灭酒精灯应该用灯帽盖灭.
(3)实验③结束时,应该先将导管从石灰水中撤出,然后熄灭酒精灯,其目的是:防止液体倒吸使试管炸裂.
(4)实验结束时,需清洗试管,整理器材.
【拓展】实验可帮助我们认识物质的性质,通过本次探究,我们认识到,铜绿的物理性质是绿色固体、难溶于水,铜绿具有的化学性质是受热易分解、能与稀盐酸反应.
【提出问题】铜绿具有什么性质?
【猜想与假设】根据网络资料,小明猜想铜绿具有如下性质:
(1)铜绿难溶于水;(2)铜绿受热分解;(3)铜绿能与稀盐酸反应.
【实验用品】铜绿、稀盐酸、澄清石灰水、药匙、试管、酒精灯、铁架台、烧杯、玻璃片、带导管的单孔塞、胶头滴管、试管刷、火柴.
【实验与记录】
| 序号 | 操作 | 现象 | 结论 |
| ① | 观察铜绿的颜色、状态,取适量铜绿于试管中,加入少量的水,并振荡试管 | 铜绿是绿色、粉末状固体,难溶于水 | 猜想(1)正确 |
| ② | 小心将实验①试管中的水倾出,但不要倒出固体,往试管中加入适量的稀盐酸 | 滴加稀盐酸后,固体不断减少,最后完全消失,液体变成蓝色 | 猜想(3) 正确 |
| ③ | 另取适量铜绿于试管中,带上带导管的胶塞,将试管固定在铁架台上,将导管另一端伸入盛有澄清石灰水的试管中,然后用酒精灯加热盛有铜绿的试管 | 加热一段时间后,固体由绿色变成黑色,澄清的石灰水变浑浊 | 猜想(2) 正确 |
(1)本次探究中,涉及取用药品.粉末状固体取用的操作,将试管竖直放置,用药匙将铜绿从试管口倒入试管中,可能带来的后果是药品附着在试管壁上.
(2)酒精灯时化学实验常见的热源,加热时应该利用酒精灯的外焰加热,熄灭酒精灯应该用灯帽盖灭.
(3)实验③结束时,应该先将导管从石灰水中撤出,然后熄灭酒精灯,其目的是:防止液体倒吸使试管炸裂.
(4)实验结束时,需清洗试管,整理器材.
【拓展】实验可帮助我们认识物质的性质,通过本次探究,我们认识到,铜绿的物理性质是绿色固体、难溶于水,铜绿具有的化学性质是受热易分解、能与稀盐酸反应.
3. 如图所示是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图.下列说法错误的是( )
如图所示是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图.下列说法错误的是( )
 如图所示是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图.下列说法错误的是( )
如图所示是盐酸滴入氢氧化钠溶液中,有关粒子之间反应的示意图.下列说法错误的是( )| A. | 盐酸溶液中只含有氢离子、氯离子 | |
| B. | 两种溶液混合时,氢离子和氢氧根离子结合生成水 | |
| C. | 表示盐酸与氢氧化钠溶液恰好完全中和 | |
| D. | 两种溶液混合前后,钠离子和氯离子没有发生变化 |




