题目内容
2. 实验室中某瓶浓盐酸的标签如图所示.请根据有关信息计算:
实验室中某瓶浓盐酸的标签如图所示.请根据有关信息计算:(1)该瓶浓盐酸的质量是595g.
(2)欲配制148g溶质质量分数为5%的稀盐酸,需这种浓盐酸16.8mL.(写出计算过程)
分析 (1)从标签中的所标注的盐酸的体积和密度可以求出盐酸的质量;
(2)根据溶液稀释前后溶质的质量不变结合溶质的质量分数来解答;
解答 解:(1)从标签中可以知道盐酸的体积为500mL,密度为1.19g/cm3,可以据此求出盐酸的质量为:1.19g/cm3×500mL=595g;
(2)设需要这种浓盐酸的质量为x,根据稀释前后溶质的质量不变可知:
148g×5%=x•37%
解得:x=20g
体积为:$\frac{20g}{1.19g{/cm}^{3}}$=16.8cm3=16.8mL
故答案为:(1)595;
(2)16.8.
点评 本题考查学生利用化学方程式的计算,学生应注意通过信息抽取解题所需要的信息,能正确运用说明书中物质的体积及密度求算物质的质量.

练习册系列答案
相关题目
12.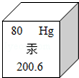 汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
 汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )| A. | 汞属于非金属元素 | B. | 汞原子核外电子数是80 | ||
| C. | 汞原子核内中子数是200.6 | D. | 汞原子的相对原子质量是120.6 |
10.下列各种物质的用途中,利用了其化学性质的是( )
| A. | 干冰用于人工降雨 | B. | 饱和氯化钠溶液用于选种 | ||
| C. | 液氮冷冻麻醉条件下做手术 | D. | 二氧化碳用作气体肥料 |
14.在盐酸、稀硫酸和稀硝酸溶液中,分别滴加石蕊试液,石蕊试夜的颜色由( )
| A. | 红变紫 | B. | 紫变红 | C. | 蓝变紫 | D. | 紫变蓝 |
5.小明家的新房装修,瓦工师傅用石灰浆(主要成分是氢氧化钙)抹墙.收工时瓦工师傅把未用完的石灰浆用沙土盖上,以备第二天再用,这样做的目的是防止石灰浆因变质而失效.
(1)小明想通过实验验证石灰浆的变质情况,请你帮助小明完成以下实验.
(2)由此小明联想到实验室里的一些药品必须密封保存.实验室中必须密封保存的药品可分为以下几类:
①药品能与空气中的成分发生反应,如澄清的石灰水;
②药品具有挥发性,如;浓盐酸③药品具有吸水性,如浓硫酸.
(1)小明想通过实验验证石灰浆的变质情况,请你帮助小明完成以下实验.
| 实验步骤 | 实验现象 | 实验结论 | |
取样,加一定量水充分溶解后,过滤 | 取少量滤渣于试管中,加入足量稀盐酸 | 有气泡产生 | 该石灰浆部分变质 |
| 取少量滤液于试管中,滴入无色酚酞试液 | 溶液变红 | ||
①药品能与空气中的成分发生反应,如澄清的石灰水;
②药品具有挥发性,如;浓盐酸③药品具有吸水性,如浓硫酸.