题目内容
10.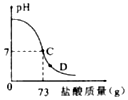 为测定某盐酸的质量分数:往20g40%的氢氧化钠溶液的烧杯中逐滴加入该盐酸,加入盐酸的质量与烧杯中溶液pH的变化关系如图所示
为测定某盐酸的质量分数:往20g40%的氢氧化钠溶液的烧杯中逐滴加入该盐酸,加入盐酸的质量与烧杯中溶液pH的变化关系如图所示(1)当滴加盐酸到图象中D点时,烧杯中溶液的溶质是NaCl、HCl(填化学式);
(2)计算该盐酸的质量分数是多少?
分析 稀盐酸和氢氧化钠反应生成氯化钠和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)当滴加盐酸到图象中D点时,稀盐酸过量,烧杯中溶液的溶质是反应生成的氯化钠和过量的氯化氢.
故填:NaCl、HCl.
(2)设恰好完全反应时73g稀盐酸中氯化氢质量为x,
NaOH+HCl═NaCl+H2O,
40 36.5
20g×40% x
$\frac{40}{20g×40%}$=$\frac{36.5}{x}$,
x=7.3g,
该盐酸的质量分数是:$\frac{7.3g}{73g}$×100%=10%,
答:该盐酸的质量分数是10%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
10.清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图(图中的微粒恰好完全反应).下列说法正确的是( )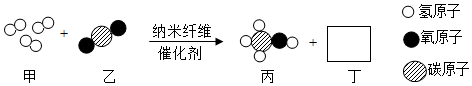

| A. | 丁的化学式为H2O,该反应为置换反应 | |
| B. | 参加反应的甲与乙的质量比为3:1 | |
| C. | 甲是单质,乙、丙、丁均为氧化物 | |
| D. | 该反应体现了无机物可以转化为有机物 |
5.通过下列实验操作和现象得出的结论,合理的是
| 实验操作 | 现象 | 结论 | |
| A | 把铜片放入硝酸银溶液中 | 出现白色固体 | 铜比银化学性质活泼 |
| B | 向某白色粉末中滴加适量稀盐酸 | 白色粉末消失,产生气泡 | 白色粉末是Na2CO3 |
| C | 50℃时,将17gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为17g |
| D | 将氢氧化钠固体加入水中 | 溶液温度升高 | 该反应放热 |
| A. | A | B. | B | C. | C | D. | D |
2.乳酸亚铁可用于治疗缺铁性贫血.已知乳酸亚铁的化学式为C6H10FeO6.下列关于乳酸亚铁说法正确的是( )
| A. | 由三种非金属和一种金属组成 | B. | 属于氧化物 | ||
| C. | 含有5个氢分子 | D. | C6H10FeO6中C、O的质量比为3:4 |
19.最近科学家研究发现了一种新的固态碳结钢形式“Q-carbon”,该结构的材料能够在常温常压下制备钻石.下列关于“Q-carbon”的说法正确的是( )
| A. | 它与金刚石的物理性质相同 | B. | 它里面的碳原子静止不动 | ||
| C. | 它是一种新型的碳的化合物 | D. | 它的结构不同于石墨 |
20.下列说法中,正确的是( )
| A. | NaNO2中氮元素的化合价是+1 | B. | 甲醛水溶液可用于海产品保鲜 | ||
| C. | 人体内缺少铁元素会引起贫血 | D. | 食用蔬菜、水果可大量补充蛋白质 |