题目内容
2002年3月,我国自行研制的“长征二号”捆绑式火箭将“神州三号”正样飞船送上了太空.火箭的主要燃料叫“偏二甲肼”,已知该化合物的化学式的相对分子质量为60,其中碳、氢元素的质量分数分别是40.00%和13.33%,其余为氮元素,则
(1)偏二甲肼的化学式为 .
(2)在火箭发射时,偏二甲肼和四氧化二氮(N2O4)发生剧烈反应,释放出大量的热量,并产生大量氮气、二氧化碳和水蒸气.请写出该反应的化学方程式: .
(1)偏二甲肼的化学式为
(2)在火箭发射时,偏二甲肼和四氧化二氮(N2O4)发生剧烈反应,释放出大量的热量,并产生大量氮气、二氧化碳和水蒸气.请写出该反应的化学方程式:
考点:化合物中某元素的质量计算,书写化学方程式、文字表达式、电离方程式
专题:化学式的计算,化学用语和质量守恒定律
分析:(1)根据化学式中元素质量分数的计算方法分析;
(2)根据反应写出反应的化学方程式.
(2)根据反应写出反应的化学方程式.
解答:解:(1)偏二甲肼分子中碳原子的个数是:
=2;氢原子的个数是:
=8;
氮原子的个数是:
=2.所以化学式是:C2H8N2;
(2)在火箭发射时,偏二甲肼和四氧化二氮(N2O4)发生剧烈反应,释放出大量的热量,并产生大量氮气、二氧化碳和水蒸气.该反应的化学方程式:C2H8N2+2N2O4
2CO2+4H2O+3N2.
故答为:(1)C2H8N2;(2)C2H8N2+2N2O4
2CO2+4H2O+3N2.
| 60×40% |
| 12 |
| 60×13.33% |
| 1 |
氮原子的个数是:
| 60×(1-40%-13.33%) |
| 14 |
(2)在火箭发射时,偏二甲肼和四氧化二氮(N2O4)发生剧烈反应,释放出大量的热量,并产生大量氮气、二氧化碳和水蒸气.该反应的化学方程式:C2H8N2+2N2O4
| ||
故答为:(1)C2H8N2;(2)C2H8N2+2N2O4
| ||
点评:本题难度不大,考查学生根据化学式的计算、写化学方程式的能力.化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
下列各组溶液,不加其他试剂就能鉴别的是( )
| A、K2SO4、BaCl2、Na2CO3、HCl |
| B、HNO3、Na2CO3、Ca(NO3)2、HCl |
| C、CuCl2、K2SO4、NaNO3、NaOH |
| D、AgN03、KCl、NaCl、HNO3 |
下列四个图象中,不能正确表示对应变化关系的是( )
A、 加热氯酸钾和二氧化锰的混合物 |
B、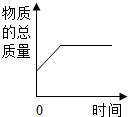 密闭容器中点燃红磷 |
C、 加热氯酸钾和二氧化锰的混合物 |
D、 密闭容器中点燃红磷 |
下列变化属于化学变化的是( )
| A、石蜡熔化 | B、煤球燃烧 |
| C、铁丝弯曲 | D、海水晒盐 |
有毒的工业用盐亚硝酸钠NaNO2常被一些人误作食盐用于烹调而造成中毒事故.其中氮元素化合价与下列那种物质中氮元素的化合价相同( )
| A、氨气 | B、硝酸 |
| C、二氧化氮 | D、三氧化二氮 |
用蒸馏水配成的某盐溶液,加入硝酸使溶液显酸性,再加入氯化钡溶液时,有白色沉淀生成,对此盐的下列判断中正确的是( )
| A、肯定不是Na2CO3 |
| B、肯定是Na2SO4 |
| C、肯定是AgNO3 |
| D、肯定是硫酸盐 |