题目内容
铁、钢是我们生活中重要的金属材料.
(1)下列生活用品中,铁锅用来做饭是利用了铁的 性,钢丝作导线是利用了铜的 性.
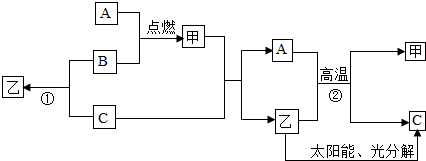
(2)根据如图转化关系图1,回答问题.
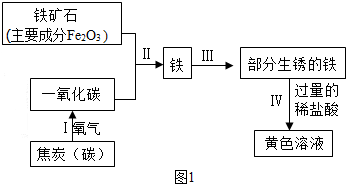
①铁生锈的条件是 .
②写出步骤Ⅱ中的化学方程式 .
③黄色溶液中的溶质是 .
④回收再利用生锈的铁制品是保护金属资源的一种有效途径.如图所示的废铁粉中Fe2O3含量大约在80%左右(其余20%为铁),若回收100t这样的废铁粉可以得到 t铁.
(3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用.欲从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部铜.处理过程如图2:
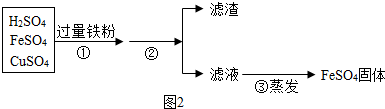
步骤①加入过量铁粉,发生的反应方程式为: , .充分反应后步骤②进行的操作是 ,得到的滤渣中含有 ,继续处理可以得到纯净的金属铜和硫酸亚铁固体.
(1)下列生活用品中,铁锅用来做饭是利用了铁的
(2)根据如图转化关系图1,回答问题.

①铁生锈的条件是
②写出步骤Ⅱ中的化学方程式
③黄色溶液中的溶质是
④回收再利用生锈的铁制品是保护金属资源的一种有效途径.如图所示的废铁粉中Fe2O3含量大约在80%左右(其余20%为铁),若回收100t这样的废铁粉可以得到
(3)矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用.欲从含有硫酸、硫酸亚铁和硫酸铜的废液中,回收全部铜.处理过程如图2:

步骤①加入过量铁粉,发生的反应方程式为:
考点:金属的物理性质及用途,金属的化学性质,铁的冶炼,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)金属具有良好的导电性和导热性,因此在现实生活中有着广泛的用途;
(2)①铁的生锈是金属与氧气和水共同作用的结果;
②一氧化碳与氧化铁反应会生成铁与二氧化碳;
③从生锈的铁与过量盐酸的反应产物进行判断;
④根据题意,由废铁粉中Fe2O3含量大约在80%左右(其余20%为铁),回收100t这样的废铁粉,由化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
(3)根据反应物和生成物及其质量守恒定律可以书写化学方程式;过滤可以把不溶于水的物质除去;铁能和稀硫酸反应生成氢气.
(2)①铁的生锈是金属与氧气和水共同作用的结果;
②一氧化碳与氧化铁反应会生成铁与二氧化碳;
③从生锈的铁与过量盐酸的反应产物进行判断;
④根据题意,由废铁粉中Fe2O3含量大约在80%左右(其余20%为铁),回收100t这样的废铁粉,由化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
(3)根据反应物和生成物及其质量守恒定律可以书写化学方程式;过滤可以把不溶于水的物质除去;铁能和稀硫酸反应生成氢气.
解答:解:(1)由于金属具有良好的导热性与导电性,所以铁可以制成铁锅,铜可以制成铜线;
(2)①铁的生锈主要是铁与空气中的氧气与水综合反应的结果;
②一氧化碳与氧化铁反应会生成铁与二氧化碳,化学方程式为:3CO+Fe2O3
2Fe+3CO2;
③生锈的铁中的氧化铁与铁分别于盐酸反应会生成氯化铁与氯化亚铁另外还会有剩余的盐酸,因此含有的溶质是:FeCl2、FeCl3、HCl;
④根据题意,由废铁粉中Fe2O3含量大约在80%左右,100t这样的废铁粉含80%Fe2O3中含铁元素的质量为100t×80%×
×100%=56t,100t这样的废铁粉中含铁元素的质量为100t×20%=20t;故回收100t这样的废铁粉可以得到铁的质量为56t+20t=76t;
(3)铁与硫酸、硫酸铜都能反应,铁与硫酸反应生成硫酸亚铁和氢气,化学方程式为:H2SO4+Fe═FeSO4+H2↑;铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═Cu+FeSO4,有金属铜析出;过滤可以把不溶于水的物质除去,得到生成的铜和过量的那部分铁.
故答案为:(1)导热,导电;
(2)①与氧气和水接触;
②3CO+Fe2O3
2Fe+3CO2;
③FeCl2、FeCl3、HCl;
④76;
(3)H2SO4+Fe═FeSO4+H2↑,Fe+CuSO4═Cu+FeSO4,过滤,铜和铁.
(2)①铁的生锈主要是铁与空气中的氧气与水综合反应的结果;
②一氧化碳与氧化铁反应会生成铁与二氧化碳,化学方程式为:3CO+Fe2O3
| ||
③生锈的铁中的氧化铁与铁分别于盐酸反应会生成氯化铁与氯化亚铁另外还会有剩余的盐酸,因此含有的溶质是:FeCl2、FeCl3、HCl;
④根据题意,由废铁粉中Fe2O3含量大约在80%左右,100t这样的废铁粉含80%Fe2O3中含铁元素的质量为100t×80%×
| 56×2 |
| 56×2+16×3 |
(3)铁与硫酸、硫酸铜都能反应,铁与硫酸反应生成硫酸亚铁和氢气,化学方程式为:H2SO4+Fe═FeSO4+H2↑;铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4═Cu+FeSO4,有金属铜析出;过滤可以把不溶于水的物质除去,得到生成的铜和过量的那部分铁.
故答案为:(1)导热,导电;
(2)①与氧气和水接触;
②3CO+Fe2O3
| ||
③FeCl2、FeCl3、HCl;
④76;
(3)H2SO4+Fe═FeSO4+H2↑,Fe+CuSO4═Cu+FeSO4,过滤,铜和铁.
点评:本题难度较大,涉及知识点较多,掌握工业上炼铁的反应原理、质量守恒定律、化学式的有关计算是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在相同温度,相同压强的条件下,气体体积之比等于气体所含分子个数之比.某混合气体中可能含有N2,CO,HCl,将其依次通过KHCO3溶液和灼热的CuO,气体体积无变化,但有红色物质生成(设各步反应均充分),再通过足量的NaOH溶液,气体体积明显减少,将燃着的木条伸入盛有剩余气体的集气瓶中,木条熄灭.则可推断该混合气体中( )
| A、一定有N2和CO,肯定无HCl |
| B、一定有N2 和CO,可能有HCl |
| C、一定有CO,HCl和N2 |
| D、一定有CO,可能有HCl和N2 |
有些地区空气污染日益严重,能形成酸雨.这是因为空气中含有较多的( )
| A、SO2 |
| B、CO |
| C、粉尘 |
| D、H2O |
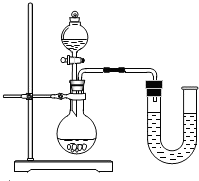 氢氧化钠与盐酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与盐酸发生了化学反应,进行了如下的实验探究.
氢氧化钠与盐酸的反应无明显现象,某化学兴趣小组为证明氢氧化钠与盐酸发生了化学反应,进行了如下的实验探究.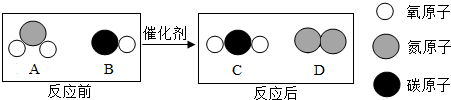
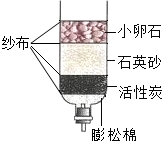 水是宝贵的自然资源,是人类生命之源.
水是宝贵的自然资源,是人类生命之源.