题目内容
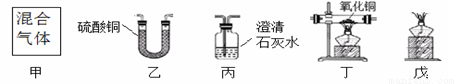
某校化学兴趣小组利用电解水、氢气燃烧、氢气还原氧化铜三组实验装置分别测定水的组成,其中图二、图三中反应所需的氢气来自实验室制氢气装置。(资料:实验室用锌粒和20%的硫酸溶液反应制取氢气,反应方程式为Zn+H2SO4 ZnSO4+H2↑)
ZnSO4+H2↑)
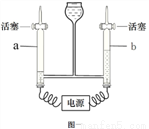
(1)按左上图一实验,写出电解水反应方程式_______,b管中产生的气体是 _______。
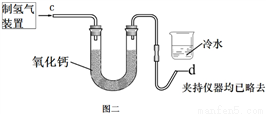
(2)按右上图二实验,图二U型管中氧化钙的作用是_______________ , 在d处点燃氢气,证明水的组成的现象是_______________________________________。
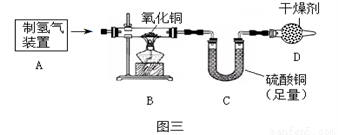
(3)按下图三实验,B装置中反应的化学方程式为______________________, C装置中的现象是 ______________。若实验测得B装置实验前后减少了3.2克,C增加了4.0克,根据实验数据计算出水中氢氧元素质量比为1:4,大于实际结果1:8,可能的原因是_______________。若B中仍有黑色固体,则实验结果_____________( 偏大,偏小,无影响),图三实验装置中D装置的作用是__________________。
 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
I.不稳定性
(1)如下图所示进行实验,过氧化氢分解的化学方程式为_______________,产生3.2g O2时分解的过氧化氢的质量为______ g。
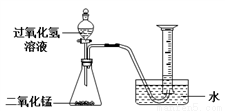
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度% | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40min | 40min | 40 min |
由此得出的结论是_____________________________。
Ⅱ.腐蚀性
【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
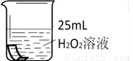
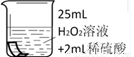
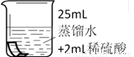
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
一段时间后的现象 | 无明显变化 | 溶液变蓝,缓慢产生细小气泡 | 无明显变化 |
【解释与结论】
(4)实验①的作用是_____________________。
(5)铜片被腐蚀的反应如下,补全该反应的化学方程式。
Cu + H2O2+ H2SO4=== CuSO4 +_______。
【反思交流】
(6)某同学提出,实验②中,除发生(5)的反应外,还发生了一个反应导致有细小气泡产生,该反应的反应物为_______。


 。
。