题目内容
11. 水和溶液在生产、生活中起着十分重要的作用,请回答下列问题.
水和溶液在生产、生活中起着十分重要的作用,请回答下列问题.(1)硬水是指含有较多可溶性钙镁化合物的水,在生活中常采用煮沸的方法降低水的硬度.
(2)NaCl、KNO3两种物质的溶解度曲线如图所示.
在20℃时,KNO3的溶解度与NaCl的溶解度相比,前者与后者的关系是C(填字母),在50℃时,KNO3溶液的溶质质量分数与NaCl溶液的溶质质量分数相比,前者与后者的关系是D(填字母).
A.大于 B.小于 C.等于 D.无法确定
(3)不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度为40℃,则t2对应的温度A(填字母)
A.大于40℃B.小于40℃C.无法确定
(4)若用溶质质量分数为16%的NaCl溶液和蒸馏水配制100g溶质质量分数为10%的NaCl溶液,则所需16%的NaCl溶液与蒸馏水的质量比为5:3.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)硬水是指含有较多可溶性钙镁化合物的水,在生活中常采用煮沸的方法降低水的硬度;
(2)在20℃时,KNO3的溶解度等于NaCl的溶解度,所以前者与后者的关系是C,在50℃时,溶液的状态不能确定,所以KNO3溶液的溶质质量分数与NaCl溶液的溶质质量分数相比,前者与后者的关系是D;
(3)气体的溶解度随温度的升高而减小,不同温度下,氧气的溶解度随压强的变化如图所示,图中t1对应的温度为40℃,则t2对应的温度大于40℃,故选A;
(4)若用溶质质量分数为16%的NaCl溶液和蒸馏水配制100g溶质质量分数为10%的NaCl溶液,需要所需16%的NaCl溶液质量为:$\frac{100g×10%}{16%}$=62.5g,需要蒸馏水的质量为:100g-62.5g=37.5g,所以所需16%的NaCl溶液与蒸馏水的质量比为62.5g:37.5g=5:3.
故答案为:(1)可溶性钙镁化合物,煮沸;
(2)C,D;
(3)A;
(4)5:3.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
2.下列物质加入到稀硫酸中,有大量气泡产生的是( )
| A. | Zn | B. | Cu | C. | K2SO4 | D. | NaOH |
19.下列图示实验操作中,正确的是( )
| A. | 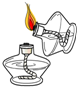 点燃酒精灯 | B. | 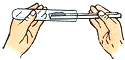 取用碳酸钠 取用碳酸钠 | C. | 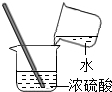 稀释浓硫酸 | D. | 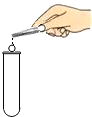 加入大理石 |
6.下列说法正确的是( )
| A. | 木炭可作冰箱除味剂 | B. | 汽油可做除去油污的乳化剂 | ||
| C. | 烧碱可作袋装食品的干燥剂 | D. | 甲醛水溶液可作食品的保鲜剂 |
16.糖类是人类食物的主要成分,下列食物中富含糖类的是( )
| A. | 蔬菜 | B. | 鸡蛋 | C. | 玉米 | D. | 豆油 |
3.下列示意图与对应的叙述正确的是( )
| A. | 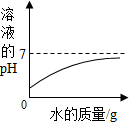 向氢氧化钠溶液中滴加足量的水 | |
| B. | 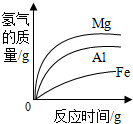 等质量的不同金属分别放入到足量的相同稀盐酸 | |
| C. | 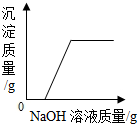 向硫酸和硫酸铜的混合溶液中滴加过量的氢氧化钠溶液 | |
| D. | 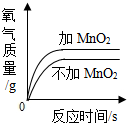 两份等体积的5%过氧化氢溶液,向其中一份加入少量二氧化锰 |
7.科学兴趣小组的同学在学了俗称为苏打的碳酸钠后,得知它还有一个俗称为小苏打的“兄弟”,这个“兄弟”的性质是否和它相似?它们之间能发生转化吗?
小明查阅了资料,将相关信息整理如表:
下面是小明同学进行的探究:
(1)用试管取适量NaHCO3溶液,向试管中滴加酚酞试液,观察试液颜色变化.此实验的目的是检验NaHCO3溶液是否显碱性.
(2)在研究Na2CO3与NaHCO3转化时,小明觉得Na2CO3转化为NaHCO3过程中,由于NaHCO3溶于水,整个过程不会有明显现象.老师笑着对小明说:“做实验吧,实验会告诉你答案.”于是小明
在老师的指导下,向饱和的Na2CO3溶液中通入CO2,起初无明显现象,继续不断地通入CO2,溶液中出现了白色沉淀.这让小明很疑惑:NaHCO3溶于水,为什么还有白色沉淀呢?小明经过思考,明白了白色沉淀产生的原因是碳酸钠与二氧化碳反应后要生成碳酸氢钠,而碳酸氢钠的溶解度小于碳酸钠,所以出现了白色沉淀.
(3)在小明同学的带动下,兴趣小组又对NaHCO3的其他性质进行了探究,发现两“兄弟”既有相似的性质也有不同的个性.从微观角度分析,造成两“兄弟”不同个性的原因是酸根离子不同.
小明查阅了资料,将相关信息整理如表:
| 俗名 | 苏打 纯碱 | 小苏打 |
| 化学式 | Na2CO3 | NaHCO3 |
| 构成微粒 | Na+ CO32- | Na+ HCO3- |
| 溶解度(常温) | 21.5克 | 9.6克 |
| 两者的转化 | Na2CO3+CO2+H2O═2NaHCO3 | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2+H2O |
(1)用试管取适量NaHCO3溶液,向试管中滴加酚酞试液,观察试液颜色变化.此实验的目的是检验NaHCO3溶液是否显碱性.
(2)在研究Na2CO3与NaHCO3转化时,小明觉得Na2CO3转化为NaHCO3过程中,由于NaHCO3溶于水,整个过程不会有明显现象.老师笑着对小明说:“做实验吧,实验会告诉你答案.”于是小明
在老师的指导下,向饱和的Na2CO3溶液中通入CO2,起初无明显现象,继续不断地通入CO2,溶液中出现了白色沉淀.这让小明很疑惑:NaHCO3溶于水,为什么还有白色沉淀呢?小明经过思考,明白了白色沉淀产生的原因是碳酸钠与二氧化碳反应后要生成碳酸氢钠,而碳酸氢钠的溶解度小于碳酸钠,所以出现了白色沉淀.
(3)在小明同学的带动下,兴趣小组又对NaHCO3的其他性质进行了探究,发现两“兄弟”既有相似的性质也有不同的个性.从微观角度分析,造成两“兄弟”不同个性的原因是酸根离子不同.
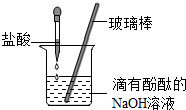 某同学用盐酸与氢氧化钠按照如图的方式进行中和反应实验.
某同学用盐酸与氢氧化钠按照如图的方式进行中和反应实验.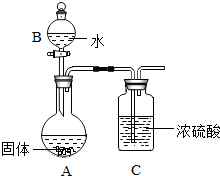 同学们利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成,甲组同学取一定量燃烧后的固体投入水中.生成碱的同时得到一种能使湿润红色石蕊试纸变蓝的气体,说明固体中含有Mg3N2,生成该气体的化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.
同学们利用镁在空气中燃烧后的固体(不含单质)进行实验,探究其组成,甲组同学取一定量燃烧后的固体投入水中.生成碱的同时得到一种能使湿润红色石蕊试纸变蓝的气体,说明固体中含有Mg3N2,生成该气体的化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.