题目内容
如图所示,A~F是初中化学常见的物质,其中A是紫红色金属,B、E常温下均是气体,E、F都能用于灭火,C是人体胃液中含有的酸。图中“—”表示物质间能发生化学反应,“→”表示物质间的转化关系。请回答:
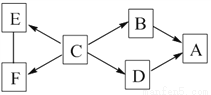
(1)A的一种用途是______________。
(2)B、E的化学式分别为______、______。
(3)D→A的化学方程式为______________。
制作导线等 H2、 CO2 Fe+CuCl2FeCl2+Cu(合理即可) 【解析】根据所学知识和题中信息知,A是紫红色金属,A是铜,B、E常温下均是气体,E、F都能用于灭火,E是二氧化碳,B是氢气,C是人体胃液中含有的酸,C是盐酸,D是氯化铜。(1)A的一种用途是制作导线等,铜具有良好的导电性。(2)B、E的化学式分别H2、CO2。(3)D→A的化学方程式为. Fe+CuCl2=FeCl2+...某化学兴趣小组有一次活动的内容是:对一包干燥的红色粉末组成进行探究。请你参与并回答有关问题。
【教师提醒】:它由Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成。
【提出猜想:】红色粉末可能的组成有: ①只有Cu;②只有Fe2O3;③只有Fe(OH)3;④是Fe2O3、Fe(OH)3的混合物;⑤是Cu、Fe2O3的混合物;⑥是Cu、Fe(OH)3的混合物。
【资料获悉】:
(1)氢氧化铁受热分解为氧化铁和水。(2)白色无水硫酸铜遇水变蓝。
(3)氧化铁可以和稀盐酸反应生成氯化铁和水。
(4)铜在黄色氯化铁溶液中可以发生反应生成氯化亚铁和氯化铜。
【探究思路】:利用物质的性质不同设计实验加以甄别,先分别探究其中是否含有Fe(OH)3, Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究其组成。 (装置内空气中的水蒸气、二氧化碳忽略不计)
【实验探究】:
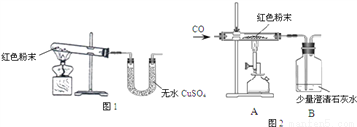
(1)甲同学取适量红色粉末装入试管中,按图1进行实验。结果无水硫酸铜没有变蓝,从而排除猜想中的_________。(填猜想中的序号)
(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色。乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为_________的观点正确(填"乙"或"丙")。
(3)丁同学为进一步确定红色粉末的组成,称取5.0g该粉末装入硬质玻璃管中,按图2在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
组别 | 反应前 | 反应后 |
Ⅰ组 | 玻璃管和红色粉末总质量为37.3g | 玻璃管和固体物质总质量为36.1g |
Ⅱ组 | 洗气瓶和所盛溶液总质量为180.0g | 洗气瓶和物质总质量为183.1g |
【交流讨论】:
(1)在装置中先通CO气体的作用是________。
(2)应该选择_________组的实验数据计算来确定红色粉末的组成。最终计算结果表明:该红色粉末的组成是猜想中的第_________组(填序号)。
(3)实验中观察到A装置中的现象为___________。
(4)为了防止溶液倒吸,本实验停止加热前是否需要先断开A和B的连接处?_______(填"需要"或"不需要"),理由是________。
【反思评价】:从环保角度,图二缺少尾气处理装置。
346 丙 排尽装置中空气,防止爆炸。 Ⅰ 5 部分红色粉末变黑 不需要 实验结束后,一直在通一氧化碳 【解析】本题主要对炼铁的实验原理、实验现象、操作步骤、装置连接及实验分析与评价等方面进行考查。熟练掌握该实验的反应原理以及实验注意事项是解决此类问题的关键。 实验探究: (1)根据提供的资料:氢氧化铁受热分解为氧化铁和水,白色无水硫酸铜遇水变蓝。加热红色粉末,结果无水CuSO4...



