题目内容
2.总结化学规律要严谨、科学.下列说法中正确的是( )| A. | 酸溶液中一定含有氢离子 | |
| B. | 气体受热膨胀是因为温度升高气体分子变大 | |
| C. | 生成盐和水的反应一定是中和反应 | |
| D. | 铝合金、塑料、玻璃钢都是复合材料 |
分析 A、根据酸溶液的特点分析;
B、根据分子间有间隔的性质分析;
C、根据中和反应的定义分析;
D、根据材料的特点分析.
解答 解:A、酸是解离出的阳离子都是氢离子的化合物,因此酸溶液中一定含有氢离子.故A正确;
B、气体受热膨胀是因为温度升高气体分子的间隔变大,分子的体积不变,故B错误;
C、生成盐和水的反应不一定是中和反应,必需是酸与碱作用生成盐和水的反应,故C错误;
D、铝合金属于金属材料,塑料属于有机合成材料,故D错误.
故选A.
点评 本题主要考查了在化学中的一些概念的严密性,定义正说是对的,但反过来说就不一定对了,要注意叙述的严密性.掌握酸性溶液的特征、分子的性质、中和反应的定义、溶液浓稀与饱和溶液、不饱和溶液的关系是解题的关键.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
12.某食品包装中充有某种气体如图1.实验小组的同学想对该气体的主要成分进行研究.
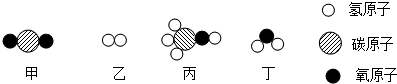
猜想:甲同学认为可能为氮气,乙同学认为可能为二氧化碳,丙同学认为是氮气和二氧化碳的混合物.
为了进一步研究该气体成分,实验小组的同学进行了如下的探究:
探究一:
探究二:用图2装置继续进行实验(假设每步都完全反应):
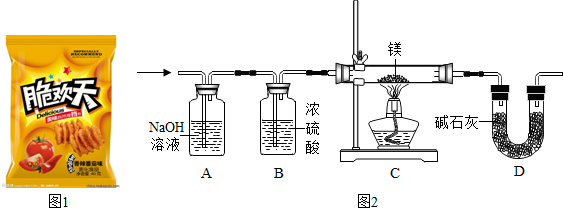 (1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(2)同学们将C装置中淡黄色固体取出,加入水中,产生一种不溶性碱和能使湿润的红色石蕊试纸变为蓝色的气体,则氮化镁与水反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.通过以上实验探究可以得出:该气体组成为N2和CO2.
猜想:甲同学认为可能为氮气,乙同学认为可能为二氧化碳,丙同学认为是氮气和二氧化碳的混合物.
为了进一步研究该气体成分,实验小组的同学进行了如下的探究:
探究一:
| 实验操作 | 实验现象 | 实验结论 |
| 把气体通入澄清的石灰水溶液中. | 产生白色沉淀 | 甲同学的猜想不正确,该过程中发生反应的方程式为:Ca(OH)2+CO2=CaCO3↓+H2O. |
 (1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
(1)点燃酒精灯前先通一会儿该气体,其作用是赶出装置内的空气,B装置中浓硫酸的作用是除去气体中的水蒸气,C装置中产生的一种淡黄色的固体为氮化镁(Mg3N2),发生反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.(2)同学们将C装置中淡黄色固体取出,加入水中,产生一种不溶性碱和能使湿润的红色石蕊试纸变为蓝色的气体,则氮化镁与水反应的化学方程式为Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑.通过以上实验探究可以得出:该气体组成为N2和CO2.
10.下列说法或做法错误的是( )
| A. | C02和C在高温下反应生成CO,在该反应中C02表现出了氧化性 | |
| B. | 实验室制取C02时,先证明气体是否收集满了,然后再检验气体是不是CO2 | |
| C. | 汽油、天然气等燃烧引起的火灾可用干粉灭火器来扑灭 | |
| D. | C、H2、CO三种物质具有一些相似的化学性质 |
14.生活中的下列物质不属于溶液的是( )
| A. | 雪碧 | B. | 白醋 | C. | 白酒 | D. | 奶茶 |
11.摘录某同学实验记录本中有关实验现象的记录,其中肯定有误的是( )
| A. | 硫在氧气中燃烧,会产生明亮的蓝紫色火焰,产生有刺激性气味的气体 | |
| B. | 在空气中打开浓盐酸的瓶盖,有刺激性气味,产生白烟 | |
| C. | 点燃一氧化碳时,会产生蓝色火焰,产物能使石灰水变浑浊 | |
| D. | 木炭在氧气中燃烧比在空气中更旺,发出白光,并且放热 |