题目内容
不纯的NaCl样品中可能含有KCl、MgCl2、NaNO3中的一种或几种.称取11.7g样品加到水中,得到无色溶液,向其中滴加过量的AgNO3溶液,得到28.7g白色沉淀,则NaCl样品的可能组成是:
① ;② ;③ .
①
考点:根据化学反应方程式的计算,盐的化学性质
专题:推断混合物的可能组成
分析:可以假设样品是纯净的氯化钠,计算出与硝酸银反应生成氯化银沉淀的质量,然后再根据杂质中氯元素的含量,可以判断出样品的组成.
解答:解:氯化钠中氯元素的质量分数为:
×100%=60.7%;
氯化钾中氯元素的质量分数为:
×100%=47.7%;
氯化镁中氯元素的质量分数为:
×100%=74.7%;
硝酸钠中不含有氯元素.
设纯净的氯化钠11.7g与足量的硝酸银反应生成沉淀氯化银的质量为x,
NaCl+AgNO3═AgCl↓+NaNO3,
58.5 143.5
11.7g x
=
,
x=28.7g,
所以样品中一定含有比氯化钠中氯元素含量高的物质,也一定含有比氯化钠中氯元素含量低的物质;
则NaCl样品的可能组成是:NaCl,KCl、MgCl2,或NaCl,MgCl2,NaNO3,或NaCl,KCl,MgCl2,NaNO3.
故填:NaCl,KCl、MgCl2;NaCl,MgCl2,NaNO3;NaCl,KCl,MgCl2,NaNO3.
| 35.5 |
| 58.5 |
氯化钾中氯元素的质量分数为:
| 35.5 |
| 74.5 |
氯化镁中氯元素的质量分数为:
| 71 |
| 95 |
硝酸钠中不含有氯元素.
设纯净的氯化钠11.7g与足量的硝酸银反应生成沉淀氯化银的质量为x,
NaCl+AgNO3═AgCl↓+NaNO3,
58.5 143.5
11.7g x
| 58.5 |
| 11.7g |
| 143.5 |
| x |
x=28.7g,
所以样品中一定含有比氯化钠中氯元素含量高的物质,也一定含有比氯化钠中氯元素含量低的物质;
则NaCl样品的可能组成是:NaCl,KCl、MgCl2,或NaCl,MgCl2,NaNO3,或NaCl,KCl,MgCl2,NaNO3.
故填:NaCl,KCl、MgCl2;NaCl,MgCl2,NaNO3;NaCl,KCl,MgCl2,NaNO3.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于绿色化学的表述中,其中有严重错误的是( )
| A、绿色化学是要充分利用资源和能源,采用无毒、无害的原料 |
| B、绿色化学就是生产不含化学成分的物质 |
| C、绿色化学是要提高原子利用率,力图使原料的原子都被产品所消纳,实现“零现放” |
| D、绿色化学核心就是要利用化学原理从源头消除污染 |
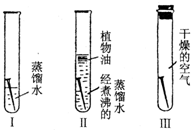 为探究铁锈蚀的原因,某学习小组进行了如下实验:将三枚无锈铁钉分别放入三支试管中(如图),数天后,只有试管I中的铁钉在水面处生锈,其它两支试管中的铁钉没有发生变化.请回答下列问题:
为探究铁锈蚀的原因,某学习小组进行了如下实验:将三枚无锈铁钉分别放入三支试管中(如图),数天后,只有试管I中的铁钉在水面处生锈,其它两支试管中的铁钉没有发生变化.请回答下列问题: