题目内容
4.化学是一门以实验为基础的科学,根据实验1、实验2回答下列问题:
(1)看实验1,将一瓶二氧化碳气体沿烧杯左侧内壁缓慢倒入,观察到的现象是蜡烛由下至上依次熄灭,这一现象说明二氧化碳(答一条即可)二氧化碳既不能燃烧也不能支持燃烧(或二氧化碳密度比空气大).
(2)看实验2,说明浓硫酸具有腐蚀(或脱水)性,因此,在取用浓硫酸时,要特别小心,如果不心将浓硫酸沾到皮肤上,正确的处理方法是先用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液,其中第二步处理的原理是(用化学方程式表示)2NaHCO3+H2SO4=Na2SO4+2H2O+CO2↑.
分析 (1)二氧化碳的密度比空气大,不燃烧也不支持燃烧;
(2)浓硫酸属于酸,所以具有酸性,浓硫酸浓度较高,所以还有脱水性及吸水性,据此分析解答.
解答 解:(1)将一瓶二氧化碳气体沿烧杯左侧内壁缓慢倒入,观察到的现象是:燃着的蜡烛由下至上依次熄灭;这些现象说明二氧化碳具有的性质是:二氧化碳的密度比空气大;不能燃烧,不支持燃烧;
(2)浓硫酸具有脱水性,纸张的主要成分是纤维素,浓硫酸能将纸张中H、O元素以2:1水的形式脱去,最终生成炭黑,所以该实验体现了浓硫酸的脱水性,浓硫酸具有强烈的腐蚀性,不慎沾到皮肤上,应立即用大量清水冲洗,后涂上3%~5%的碳酸氢钠溶液.碳酸氢钠与稀硫酸反应生成硫酸钠、水、二氧化碳,反应的化学方程式为:2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O.
故答案是:(1)蜡烛由下至上依次熄灭; 二氧化碳既不能燃烧也不能支持燃烧(或二氧化碳密度比空气大);
(2)腐蚀(或脱水);先用大量的水冲洗,再涂上3%-5%的碳酸氢钠溶液;2NaHCO3+H2SO4=Na2SO4+2H2O+CO2↑
点评 本考点主要考查气体了二氧化碳、浓硫酸的性质,同时也考查了化学方程式的书写,综合性比较强.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
1.下列有关溶液的叙述错误的是( )
| A. | 溶液中的溶剂只能是水 | |
| B. | 固体NaOH溶于水时,溶液温度升高 | |
| C. | 一定条件下,饱和溶液和不饱和溶液可以相互转化 | |
| D. | 溶液是均一、稳定的混合物 |
2.根据化合价由高到低的顺序,在HClO4、NaClO3、HCl0、( )、NaCl的排列中,括号内应填入下列物质中的是( )
| A. | Cl2 | B. | HClO3 | C. | Cl2O7 | D. | HCl |
19.甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:
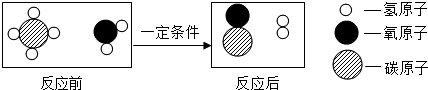
根据以上微观示意图得出的结论中,正确的是( )

根据以上微观示意图得出的结论中,正确的是( )
| A. | 反应前后各元素的化合价均不变 | |
| B. | 水煤气的成分是一氧化碳和氧气 | |
| C. | 该反应中含氢元素的化合物有3种 | |
| D. | 该反应的化学方程式中,反应物甲烷和水的计量数之比为1:1 |
9.食醋是生活中重要的调味品,对食醋的描述与其物理性质有关的是( )
| A. | 醋瓶被打翻后,室内醋味十足 | |
| B. | 可除去热水瓶中的水垢 | |
| C. | 被某些虫子叮咬,涂食醋能消肿解毒 | |
| D. | 进餐时,鱼刺、骨头若卡在咽喉处,可用醋使鱼刺骨软化而不致发生危险 |
16.生活中有太多的变化,下列“变”中只涉及物理变化的是( )
| A. | 积雪“变”水 | B. | 葡萄“变”美酒 | C. | 米饭“变”馊 | D. | 纸燃烧“变”灰烬 |
13.雾霾严重影响人们的生活和健康.某地区的雾霾中可能含有如下可溶性物质NH4NO3、NaNO3、BaCl2、MgCl2、Na2SO4中的一种或多种,该地区的雾霾,经必要的处理后得到试样溶液,设计并完成了如图所示实验.
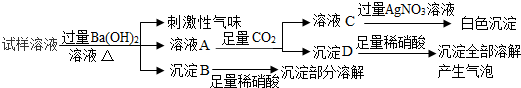
根据以上实验操作与现象,该同学得出的结论错误的是( )

根据以上实验操作与现象,该同学得出的结论错误的是( )
| A. | 沉淀B的化学式Mg(OH)2和BaSO4 | |
| B. | 沉淀D的化学式为BaCO3 | |
| C. | 试样溶液中一定不含有NaNO3和BaCl2 | |
| D. | 试样溶液中一定含有NH4NO3、MgCl2、Na2SO4 |
14.碳酸钾是农家肥草木灰的主要成分,将它和化肥一起施用,会减少对环境的污染.为了帮助父母合理选择化肥,李明决定对碳酸钾的化学性质进行探究.
【提供信息】钠原子和钾原子的结构示意图分别为:

【实验与探究】李明参照Na2CO3的化学性质设计了如下实验:
【解释与结论】
(1)碳酸钾溶液能使指示剂变色,能与某些酸和碱反应;
(2)碳酸钾与碳酸钠的化学性质相似:
(3)从微观角度分析,二者化学性质相似的原因是易溶于水和含有相同的CO32-;
【拓展与应用】李明建议父母最好选择B(填字母序号)与草木灰混合施用
A.NH4NO3 B.CO(NH2)2 C.NH4HCO3.
【提供信息】钠原子和钾原子的结构示意图分别为:

【实验与探究】李明参照Na2CO3的化学性质设计了如下实验:
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 实验步骤 |  |  |  |
| 实验现象 | 溶液变红色 | 左边试管中有气泡产生澄清石灰水变浑浊 | 产生白色沉淀 |
| 实验结论 | 碳酸钾溶液显碱性 | 产生气泡的化学方程式为K2CO3+2HCl═2KCl+H2O+CO2↑ | 碳酸钾能与氢氧化钙溶液反应 |
(1)碳酸钾溶液能使指示剂变色,能与某些酸和碱反应;
(2)碳酸钾与碳酸钠的化学性质相似:
(3)从微观角度分析,二者化学性质相似的原因是易溶于水和含有相同的CO32-;
【拓展与应用】李明建议父母最好选择B(填字母序号)与草木灰混合施用
A.NH4NO3 B.CO(NH2)2 C.NH4HCO3.
