题目内容
5.华雪同学制作“叶脉书签”,需要50g质量分数为10%的氢氧化钠溶液.回答下列问题:(1)若用氢氧化钠固体配制所需溶液,需称取氢氧化钠固体5g;
(2)配制的步骤可以概括为计算、称量和量取、溶解、装瓶贴标签;
(3)所需玻璃仪器有量筒、滴管、烧杯、玻璃棒,其中玻璃棒的作用是加快氢氧化钠固体的溶解速率.
(4)在配制一定质量分数的氢氧化钠溶液时,下列出现的操作失误,会引起所配溶液中溶质的质量分数偏小的是AC.
A、用量筒量取蒸馏水,读数时仰视凹液面的最低处.
B、将量筒中的水倒入烧杯时,有少量水洒出.
C、氢氧化钠固体中含有杂质.
D、将配好的氢氧化钠溶液转移到细口瓶中时,不慎洒出部分溶液.
分析 (1)根据溶质质量=溶液质量×溶质质量分数计算;
(2)根据配制的步骤可以概括为计算、称量和量取、溶解、装瓶贴标签进行分析;
(3)根据需要的玻璃仪器有:烧杯、量筒、玻璃棒;玻璃棒的作用是搅拌加速氢氧化钠溶解进行分析;
(4)根据溶质质量分数降低需要从溶质少了,溶剂多了考虑.
解答 解:(1)氢氧化钠的质量:50g×10%=5g;
(2)配制的步骤可以概括为计算、称量和量取,溶解,装瓶存放;
(3)需要的玻璃仪器有:烧杯、量筒、玻璃棒;玻璃棒的作用是搅拌加速氢氧化钠溶解;
(4)溶质质量分数降低可能是由于溶质少了或溶剂多了考虑,
A.用量筒量取蒸馏水读数时,仰视凹液面的最低处,量取的水多了,所以溶质质量分数偏小;
B.将量筒中的水倒入烧杯时,有水洒出,说明溶剂少了,所以溶质质量分数偏大;
C.氢氧化钠中含有杂质说明称量的氢氧化钠质量少了,所以溶质质量分数偏小;
D.将配好的氢氧化钠溶液转移到细口瓶中时,不慎洒出部分溶液,此时溶液已经配好了,洒出后溶质质量分数不变,因为溶液是均一的.
故选:AC.
故答案为:(1)5g;
(2)溶解;
(3)量筒、滴管、烧杯、玻璃棒,加快氢氧化钠固体的溶解速率;
(4)A、C.
点评 熟练掌握溶质质量分数的计算公式和公式变形及配制溶液的基本操作是解答该题的关键,熟悉配制溶液用到的仪器和注意事项.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.下列叙述正确的是( )
| A. | 自然界的物质都是以化合物的形式存在的 | |
| B. | 凡是含氧元素的化合物都是氧化物 | |
| C. | 只含有一种元素的物质一定是单质 | |
| D. | 混合物中含有多种物质,所以溶液一定是混合物 |
16.生物体内几乎所有的化学反应均在酶的参与下才能完成,以下有关酶的说法不正确的是( )
| A. | 酶只能在细胞内起作用 | |
| B. | 一种酶只能催化某一种或某一类化学反应 | |
| C. | 酶的催化作用受到温度、pH 的影响 | |
| D. | 酶是生物体细胞制造的一种蛋白质 |
20. 小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:
小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:
(1)猜想:瓶口的白色固体可能是碳酸钠.基于这样猜想的理由是:因为空气中含有空气中含有二氧化碳,氢氧化钠能与二氧化碳反应生成碳酸钠;
实验:他们取下一小块白色固体于试管中并加入稀盐酸,看到固体迅速溶解并产生大量气泡,从而证实了小柯的假设.
(2)请你帮他们完成验证该试剂是否已全部变质的设计方案:
(3)一定质量的NaOH溶液,变质前和变质后与盐酸反应时,所用盐酸的质量是否相同,判断并说明理由相同,因为一定质量的氢氧化钠变质程度不同,所含钠元素质量相同,相同质量的钠元素生成氯化钠时消耗氯化氢的质量相同.
 小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:
小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:(1)猜想:瓶口的白色固体可能是碳酸钠.基于这样猜想的理由是:因为空气中含有空气中含有二氧化碳,氢氧化钠能与二氧化碳反应生成碳酸钠;
实验:他们取下一小块白色固体于试管中并加入稀盐酸,看到固体迅速溶解并产生大量气泡,从而证实了小柯的假设.
(2)请你帮他们完成验证该试剂是否已全部变质的设计方案:
| 探究步骤 | 现象 | 结论 |
| ①取少量试剂于试管,向其中滴加足量的氯化钙溶液 | 产生白色沉淀 | 试剂中含有碳酸钠 |
| ②在①完全反应所得的清液中,滴加酚酞溶液 | 酚酞溶液变红 | 试剂中含有氢氧化钠 |
14.下列物质:①鸡汤②矿泉水③酒精④生理盐水⑤面汤,不属于溶液的是( )
| A. | ②④ | B. | ③④ | C. | ②③⑤ | D. | ①③⑤ |
1.与23.2kg四氧化三铁所含铁元素质量相等的三氧化二铁的质量是( )
| A. | 16kg | B. | 24kg | C. | 24.5kg | D. | 32kg |
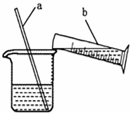 图是稀释浓硫酸实验的示意图.
图是稀释浓硫酸实验的示意图.
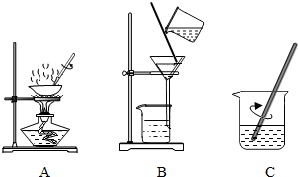
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.