题目内容
6. A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.请回答:
A-H是初中化学常见的物质,其相互转化关系如图所示,其中A是人体胃液中帮助消化的物质,B用于改良酸性土壤.请回答:(1)D的化学式为CaCl2.
(2)A转化为E的化学方程式为Fe+2HCl=FeCl2+H2↑,B转化为H的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
(3)分别写出物质F和H的一种用途供给呼吸;重要的建筑材料.
分析 此题的突破口为:A是人体胃液中帮助消化的物质,则为盐酸;B用于改良酸性土壤,因此是熟石灰氢氧化钙,C,D是A,B反应产生的,C又能通电分解,因此C是水,则D是氯化钙;C通电分解生成氢气和氧气,盐酸与活泼金属反应可以生成氢气,故E是氢气,F为氧气;B,D都能生成白色沉淀H,故H是碳酸钙;二氧化碳和氢氧化钙反应产生碳酸钙,氯化钙和碳酸钠的反应产生碳酸钙沉淀和氯化钠,然后根据反应进行推理即可.
解答 解:由于A是人体胃液中帮助消化的物质,则为盐酸;B用于改良酸性土壤,因此是熟石灰氢氧化钙,C,D是A,B反应产生的,C又能通电分解,因此C是水,则D是氯化钙;C通电分解生成氢气和氧气,盐酸与活泼金属反应可以生成氢气,故E是氢气,F为氧气;B,D都能生成白色沉淀H,故H是碳酸钙;二氧化碳和氢氧化钙反应产生碳酸钙,氯化钙和碳酸钠的反应产生碳酸钙沉淀和氯化钠;则:
(1)由分析可知D为氯化钙,故D的化学式为CaCl2;
(2)稀盐酸与活泼金属铁可以反应生成氯化亚铁和氢气,其化学方程式为Fe+2HCl=FeCl2+H2↑;
二氧化碳(碳酸钠溶液)和氢氧化钙反应产生碳酸钙和水(氢氧化钠),其化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O(或Ca(OH)2+Na2CO3=CaCO3↓+2NaOH);
(3)根据分析,F为氧气,可以共给呼吸、支持燃烧等;H为碳酸钙,可以用于建筑材料或补钙剂.
故答案为:
(1)CaCl2;
(2)Fe+2HCl=FeCl2+H2↑;Ca(OH)2+CO2=CaCO3↓+H2O(或Ca(OH)2+Na2CO3=CaCO3↓+2NaOH);
(3)供给呼吸(或支持燃烧等);重要的建筑材料(或作补钙剂等).
点评 本题属于框图式推断题,掌握常见的氧化物、酸、碱、盐的性质及常见物质的俗名及用途,学会找出题目的突破口,导出结论,最后别忘了把结论代入原题中验证.

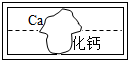 在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了一系列的探究.
在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液,同学们对该实验进行了一系列的探究.探究一 M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M物质的溶质有两种可能:
①是氢氧化钙 ②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加 酚酞 | 溶液变红 | 猜想①正确 |
【提出猜想】猜想一:NaOH 和Na2CO3; 猜想二:NaOH和Ca(OH)2;猜想三:NaOH.
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入两滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入Na2CO3溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
若A中没有沉淀,B中产生沉淀 | “猜想二”成立 | |
若AB中都没有沉淀 | “猜想三”成立 |
| A. | 水是一种常见的溶剂 | B. | 自然界中的水过滤后变成纯水 | ||
| C. | 水的蒸馏是物理变化 | D. | 地球可利用的淡水资源是有限的 |
 其中相同的球代表同种原子,说法正确的是( )
其中相同的球代表同种原子,说法正确的是( )| A. | 生成物一定是混合物 | B. | 原子在化学变化中可分 | ||
| C. | 该反应属于化合反应 | D. | 此反应的分子个数为1:1:1:1 |
| A. | 分子在不断的运动 | B. | 分子之间有间隔 | ||
| C. | 分子是由原子构成的 | D. | 分子质量很小 |
| A. | 切成小碎片 | B. | 在研钵中捣碎 | ||
| C. | 用纱布将浸泡出的汁液过滤 | D. | 在蓝色汁液中滴入盐酸变紫红色 |
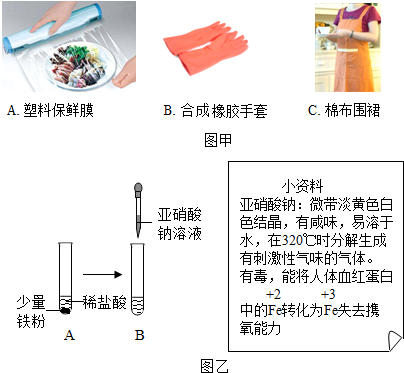
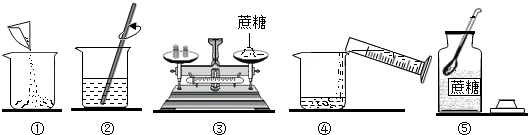
 哈尔滨市在20世纪末曾有过双层巴士(double-decker),在那之后便一度从人们的视线中消失.近日,走在大街上,双层观光巴士再一次出现了.请回答下列问题:
哈尔滨市在20世纪末曾有过双层巴士(double-decker),在那之后便一度从人们的视线中消失.近日,走在大街上,双层观光巴士再一次出现了.请回答下列问题: