题目内容
11.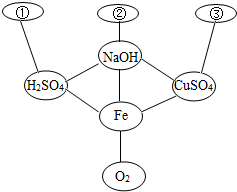 构建知识网络,理清物质间的相互关系,是科学学习中的一种重要方法.如图中连线两端的物质可以相互反应.下列四组选项中,符合该图要求的是( )
构建知识网络,理清物质间的相互关系,是科学学习中的一种重要方法.如图中连线两端的物质可以相互反应.下列四组选项中,符合该图要求的是( )| A. | ①Na2CO3 ②SO3 ③BaCO3 | B. | ①NaHCO3 ②SO2 ③KNO3 | ||
| C. | ①Fe2O3 ②CO2③Ba(NO3)2 | D. | ①CuO ②CO③HCl |
分析 根据能够和酸发生反应的物质有:活泼金属、某些金属氧化物、碱和某些盐;能够和碱发生反应的物质有:非金属氧化物、酸和某些盐;能够和盐发生反应的物质有:金属、酸、碱和盐进行分析.
解答 解:①由于能够和酸发生反应的物质除了活泼金属、碱外,还有金属氧化物(如:氧化铜、氧化铁等)和盐(如:碳酸盐、含有钡离子的可溶性盐),因此可以选这两类物质,单看①A、B、C、D都符合;
②能够和碱溶液反应的物质除了酸、盐外,只有非金属氧化物,如:二氧化碳、二氧化硫、二氧化硅、三氧化硫等,但一氧化碳不能与其反应,故排除D;
③能够和盐溶液反应的物质除了金属、碱外,还有酸和盐,但是能够和硫酸铜反应的酸没有合适的,只能选择能够和硫酸根离子结合生成沉淀的,或者是和铜离子结合生成沉淀的可溶性的盐,因此可以选择可溶性的钡盐或者是碳酸盐,而硝酸钾不能与硫酸铜反应、碳酸钡不会与硫酸铜反应,故排除A、B.
故选:C.
点评 本题难度较大,主要考查了物质间的化学反应,从而培养学生认识规律、掌握规律、应用规律的能力.

练习册系列答案
相关题目
2.铜镁合金具有优良的导电性,常用作飞机天线等导电材料.科研小组欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜合金10克放入烧杯,将140克稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量,数据记录如表.请计算:
(1)合金中镁与铜的质量比为13:7.
(2)4次实验中剩余固体减少量不相同的原因是第4次中硫酸没能完全反应.
(3)所加稀硫酸的溶质的质量分数.(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/克 | 35 | 35 | 35 | 35 |
| 剩余固体质量/克 | 9.1 | 8.2 | 7.3 | 6.5 |
(2)4次实验中剩余固体减少量不相同的原因是第4次中硫酸没能完全反应.
(3)所加稀硫酸的溶质的质量分数.(写出计算过程)
1.下列实验基本操作正确的是( )
| A. | 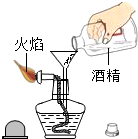 | B. | 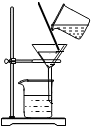 | C. | 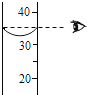 | D. | 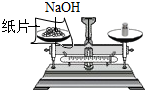 |

 某科学兴趣小组的同学在学习了空气中氧气含量的测定的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下:
某科学兴趣小组的同学在学习了空气中氧气含量的测定的基础上,改进了教材中的实验,设计出了如图所示的实验装置.实验步骤如下: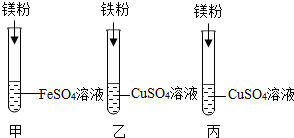 某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案:
某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案: