题目内容
除去KCl溶液中少量的K2SO4杂质,其方法是:加入适量的 溶液,反应后生成 白色沉淀再经过滤,即可除去杂质,反应的化学方程式为 .
考点:物质除杂或净化的探究,书写化学方程式、文字表达式、电离方程式
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:要除去KCl溶液中少量的K2SO4杂质,实质就是除去硫酸根离子,可利用K2SO4溶液与氯化钡溶液反应生成硫酸钡沉淀和氯化钾溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:K2SO4+BaCl2=BaSO4↓+2KCl.
故答案为:氯化钡;硫酸钡;K2SO4+BaCl2=BaSO4↓+2KCl.
故答案为:氯化钡;硫酸钡;K2SO4+BaCl2=BaSO4↓+2KCl.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
实验室收集氨气(NH3),与选择收集方法无关的信息是( )
| A、NH3的密度 |
| B、NH3的溶解性 |
| C、空气的密度 |
| D、需收集NH3的体积 |
以下燃料中属于纯净物的是( )
| A、氢气 | B、天然气 |
| C、液化气 | D、煤气 |
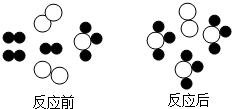 如图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中
如图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中 ,
,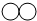 ,
, 表示A、B、C三种不同的分子.该反应的化学方程式中A、B、C前的化学计量数之比为( )
表示A、B、C三种不同的分子.该反应的化学方程式中A、B、C前的化学计量数之比为( )| A、3:1:3 |
| B、3:2:3 |
| C、3:1:2 |
| D、3:3:4 |
净化天然水的过程中一定发生化学变化的是( )
| A、蒸发 | B、挥发 | C、过滤 | D、消毒 |