题目内容
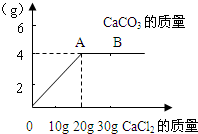 碳酸钠和氯化钠的混合物14g,在常温下溶解在足量水中,向溶液中逐滴加入氯化钙溶液,加入氯化钙的质量与生成的CaCO3沉淀的质量关系如图
碳酸钠和氯化钠的混合物14g,在常温下溶解在足量水中,向溶液中逐滴加入氯化钙溶液,加入氯化钙的质量与生成的CaCO3沉淀的质量关系如图(1)图象中表示恰好反应的点是
(2)求原混合物中氯化钠的质量分数?
分析:碳酸钠和氯化钠的混合物中的碳酸钠与所加入的氯化钙反应生成碳酸钙沉淀,随向溶液中逐滴加入氯化钙溶液质量增加,生成碳酸钙沉淀质量随之不断增加,至碳酸钠完全反应,生成沉淀的质量不再改变即曲线的A点,利用此时生成沉淀的质量,根据反应的化学方程式,计算出混合物中碳酸钠的质量即可求得原混合物中氯化钠的质量分数.
解答:解:(1)曲线A点表示生成碳酸钙的质量达最大值,即碳酸钠与所加氯化钙恰好完全反应;
(2)设混合物中Na2CO3的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl0
106 100
x 4g
=
x=4.24g
氯化钠的质量14g-4.24g=9.76g
氯化钠的质量分数=
×100%=69.71%
故答案为:(1)A;(2)69.71%.
(2)设混合物中Na2CO3的质量为x
Na2CO3+CaCl2═CaCO3↓+2NaCl0
106 100
x 4g
| 106 |
| x |
| 100 |
| 4g |
x=4.24g
氯化钠的质量14g-4.24g=9.76g
氯化钠的质量分数=
| 9.76g |
| 14g |
故答案为:(1)A;(2)69.71%.
点评:分析表示反应的曲线时,曲线的折点为所表示的反应恰好完全反应,由此点可得到恰好完全反应时反应中相关物质的质量.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (2013?泰安)小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液.他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验.
(2013?泰安)小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液.他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验.